| zurück |
2-Ethylhexylacrylat
(CAS-Nr.: 103-11-7)
Ausgabe: Januar 2006
Stand: November 1992
10 ml/m3 = 82 mg/m3
1 Substanzcharakteristik
| Substanzname: | 2-Ethylhexylacrylat |
| Synonyma: | Acrylsäure-2-ethylhexylester |
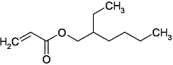
| Strukturformel: |  |
| Summenformel: | C11H20O2 |
| CAS-Nummer: | 103-11-7 |
| EG-Nummer: | 607-107-00-7 |
| BUA-Stoffliste molare Masse: | 184,3 g/mol |
| Schmelzpunkt: | -90°C |
| Siedepunkt: | 229°C |
| Flammpunkt: | 86°C |
| Dampfdruck: | 0,12 mbar |
| spezif. Gewicht: | (20°C): 0,887 g/m3 |
| Löslichkeit: | Wasser: (25°C) 0,1 g/l |
| Aussehen: | farblose Flüssigkeit |
| Umrechnungsfaktoren: | 1 ml/m3 = 8,2 mg/m3 |
| Gefährliche Reaktionen: | Vor Auslieferung wird 2-Ethylhexylacrylat gegen spontane Polymerisation stabilisiert, nach wesentlicher Überschreitung der zulässigen Lagerzeit oder Lagertemperatur kann das Projekt jedoch polymerisieren. |
2 Grenzwerte, Einstufung, Regelungen
2-Ethylhexylacrylat ist laut Anhang VI der Gefahrstoffverordnung kennzeichnungspflichtig:
| Gefahrensymbol: | Xi |
| R-Sätze: | 37/38-43 |
| S-Sätze: | - |
| zusätzlich: | 37 |
Einstufung gemäß Verordnung brennbarer Flüssigkeiten: a III Wassergefährdungsklasse: I
3 Herstellung, Verwendung, Exposition
2-Ethylhexylacrylat wird durch Veresterung von Acrylsäure mit 2-Ethylhexanol hergestellt.
Als Monomerenbaustein wird es größtenteils zur Herstellung von
Polymerdispersionen für den Bausektor und für Klebstoff eingesetzt.
4 Erfahrungen am Menschen
Sieben Probanden entwickelten im Patch-Test eine Kontaktdermatitis gegen 2-Ethylhexylacrylat und 5 der 7 Probanden darüber hinaus eine Kreuzallergie gegen Methylmethacrylat (Jordan, 1975).
Im langjährigen Umgang bei der Herstellung und bei der Weiterverarbeitung sind keine weiteren Auffälligkeiten bekannt geworden.
Lit.: Jordan, Crosssenzitization patterns in acrylat allergies. Contac Dermatitis 1, 13-15 (1975).
5 Toxikologische Daten
2-Ethylhexylacrylat zeigt im Tierversuch eine geringe akute Toxizität. Die orale LD50 an der Ratte liegt in mehreren Studien über 5.000 mg/kg [z.B. 1], die dermale Ld50 an der Ratte liegt über 12.000 mg/kg [2]. Die inhalative Exposition in einer bei 20 °C gesättigten Atmosphäre wurde von Ratten klinisch symptomlos vertragen [3]. Die Substanz zeigt an der Haut eine ausgeprägte Reizwirkung, die jedoch im Vergleich zu Acrylaten mit geringerer Kettenlänge der Alkoholkomponenten (Methyl-, Ethyl-, Butylacrylat) deutlich geringer ist [4].
2-Ethylhexylacrylat zeigte in verschiedenen Testmodellen am Meerschweinchen mit und ohne Adjuvans eine sensibilisierende Wirkung [5, 6, 7].
2-Ethylhexylacrylat zeigte im Ames-Test (mit und ohne metabolische Aktivierung) und im CHO/HGPRT-Test keine mutagene Wirkung.
Ein uneinheitliches Bild ergeben die vorliegenden Untersuchungen an weiteren Säugerzellkulturen. Negativ verlief ein Mikrokerntest an Mouse-Lymphoma-Zellen. Die Untersuchung auf Genmutationen im gleichen Versuch ergab eine nicht reproduzierbare, dosisunabhängige Erhöhung der Mutationsrate (Dearfield et al.). Ein weiterer Test (Cifone & Myhr) auf eine mögliche Genmutationenerzeugende Wirkung, ebenfalls an Mouse-Lymphoma-Zellen, ergab nach metabolischer Aktivierung einen Anstieg der Mutationsfrequenz um maximal 4,6. Allerdings wurden hier Konzentrationen getestet, die sogar höher lagen als zytotoxische Konzentrationen aus dem vorher geschilderten Versuch.
Ein fragliches Ergebnis im UDS-Test an primären Rattenhepatozyten, wird von den Autoren selbst als Effekt einer Verunreinigung diskutiert (Slesinski et al.).
Eine gentoxische Wirkung, sofern sie tatsächlich vorhanden ist, scheint erst im Bereich der Zytotoxizität aufzutreten oder direkt ursächlich an sie gekoppelt zu sein.
Demgegenüber verlief der einzig vorhandene in vivo-Test (Mikrokerntest an Mäusen) negativ.
Nachdem Untersuchungen mit dermaler Langzeitapplikation an C3H-Mäusen (DePass/Peterson) Hinweise auf ein vermehrtes Auftreten von Hauttumoren geliefert hatten, wurden an diesem Stamm umfangreiche Untersuchungen durchgeführt (Brune & Deutsch-Wenzel/WenzelHartung).
An Gruppen von je 80 männlichen C3H-Mäusen wurde bei 3maliger dermaler Gabe von 25 µg 2-Ethylhexylacrylat über die gesamte Lebensspanne in hautreizenden Testkonzentrationen von 21 bzw. 86,5 % insgesamt 39 bzw. 38 Hauttumoren gefunden (vor allem Papillome, Plattenepithelkarzinome und Melanosarkome). Bei der nicht reizenden Testkonzentration von 2,5 % waren keine Hauttumoren zu ermitteln. Eine Gruppe, die ebenfalls mit der hautreizenden Konzentration von 43 % nur 24 Wochen behandelt wurde, zeigte eine Reversibilität der Reizeffekte und am Ende der natürlichen Lebensspanne keine erhöhte Tumorinzidenz.
Vergleichende Untersuchungen ergaben, dass die verwendeten C3H-Mäuse wesentlich empfindlicher (Hautreizeffekte) auf die dermale Gabe reagierten als NMRI-Mäuse. Eine vom Aufbau vergleichbare Langzeitstudie mit diesem Stamm ergab keine hauttumorerzeugende Wirkung. Hier wurden praktisch die gleichen Konzentrationen (21,5; 43; 85 %) eingesetzt wie bei den C3H-Mäusen. Eine nach 13 Wochen getötete Satellitengruppe zeigte klinisch und histologisch nur eine leichte und nicht dosisabhängige Hautreizung, was die sehr viel stärkere Empfindlichkeit der C3H-Mäuse belegt. Nach insgesamt 7 Monaten wurde der Versuch geteilt. Während bei einem Teil der NMRI-Mäuse die dermale Applikation bis zum Versuchsende fortgesetzt wurde, erhielt der andere Teil eine 2monatige Behandlungspause. Hierauf wurde, in der Art einem Initiations-/Promotionsprotokoll vergleichbar, die bekanntermaßen hauttumorpromovierende Substanz 12-o-Tetradecanoylphorbol-13-acetat (TPA) 2mal wöchentlich dermal über 20 Wochen appliziert. Am Ende der Lebenszeit zeigten weder die kontinuierlich behandelten Tiere noch die mit dem Phorbolester promovierten Mäuse eine erhöhte Anzahl von Hauttumoren. .
Insgesamt muss die bei C3H-Mäusen aufgetretene hauttumorerzeugende Wirkung auf eine besondere Empfindlichkeit dieses Stammes in Kombination mit der lebenslangen Einwirkung deutlich hautreizender Konzentrationen zurückgeführt werden.
Systemische Effekte durch die Substanz sind wenig ausgeprägt. Zielorgane der Wirkung lassen sich nicht definieren. Dies steht in Einklang mit der relativ kurzen biologischen Halbwertszeit und der wahrscheinlich raschen Verstoffwechslung zu Alkohol und Säure mit nachfolgender Ausscheidung.
In älteren, nur eingeschränkt beurteilbaren Untersuchungen werden bei der Ratte (nur 2 Tiere pro Gruppe und Geschlecht) nach 13 x 6stündiger inhalativer Gabe ein NOEL von 50 ppm [8], bei Ratte und Maus nach täglich 5stündiger Gabe über 4 Monate ein NOEL von 48 ppm [9] angegeben.
In einer den heutigen Anforderungen entsprechenden Studie (in Anlehnung an OECD-Guideline 413) wurden je 10 Wister-Ratten pro Geschlecht und Gruppe gegenüber 0, 10, 30 und 100 ppm 2-Ethylhexylacrylat-Dämpfen arbeitstäglich für 6 Stunden über 3 Monate exponiert. 10 ppm lösten keine substanzbedingten Veränderungen aus. Bei 100 ppm und bei 30 ppm zeigte die histologische Untersuchung eine Degeneration des olfaktorischen Epithels als einzigen Befund. Bei 30 ppm waren die degenerativen Veränderungen in minimaler Intensität und nur bei etwa der Hälfte der Versuchstiere vorhanden. Auch bei einem Kontrolltier wurden minimale degenerative Veränderungen beobachtet. Klinisch fand sich in der höchsten Dosierung Lethargie und verzögerte Körpergewichtsentwicklung, korreliert mit der Veränderung klinischchemischer Parameter. Diese Veränderungen traten bei 30 ppm weniger ausgeprägt bzw. nicht auf. Die NOEC der Dampf-Inhalation von 2-Ethylhexylacrylat liegt in diesem Versuch zwischen 10 und 30 ppm, wobei die bei 30 ppm aufgetretenen Effekte als minimal charakterisiert werden.
Aufgrund der vorliegenden Untersuchungen bei der Ratte und dem dabei ermittelten NOEL bei 10 ppm unter Berücksichtigung der in ihrem Schweregrad minimalen Effekte bei 30 ppm wird ein firmeninterner Richtwert von 10 ppm abgeleitet, der infolge der sensibilisierenden Wirkung den Zusatz "S" erhält!
Bei der Übertragung der tierexperimentell ermittelten Werte auf den Menschen muss berücksichtigt werden" dass die Ratte ein obligater Nasenatmern ist und im Vergleich zum Menschen ein relativ höheres Atemminutenvolumen besitzt. Die daraus resultierende vergleichsweise hohe lokale Substanzeinwirkung an der Nase der Ratte ergibt einen ausreichenden Abstand zu einer Exposition dieses Organsystems beim Menschen.
Der Richtwert von 10 ppm für 2-Ethylhexylacrylat liegt im Bereich der für andere Acrylate aufgestellten gültigen MAK-Werte:
| Methylacrylat: | 5 ppm |
| Ethylacrylat: | 5 ppm |
| Butylacrylat: | 10 ppm |
6 Analysenmethode
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein Glasröhrchen gesaugt, das mit Aktivkohle gefüllt ist. Anschließend wird das adsorbierte 2-Ethylhexylacrylat mit Schwefelkohlenstoff desorbiert und gaschromatographisch bestimmt. |
| Bestimmungsgrenze: | absolut: 2 ng 2-Ethylhexylacrylat
relativ: 0,08 mg/m3 2-Ethylhexylacrylat bei 25 l Probeluft, 1 ml Desorptionslösung und 1 µl Injektionsvolumen |
| Selektivität: | Die Selektivität ist in jedem Einzelfall zu prüfen |
| Vorteile: | Personenbezogene und selektive Messungen möglich |
| Nachteile: | Keine Anzeige von Konzentrationsspitzen |
| Aparativer Aufwand: | Pumpe mit Gasmengenzähler oder Volumenstromanzeiger, Adsorptionsröhrchen, Gaschromatograph mit Flammenionisations-Detektor |
Literatur:
[1] Sandmeier, E.E. und Kirvin jr. C.J. (1981) in: Patty's Industrial Hygiene and Toxicology, Ed. Clayton, G.D. und Clayton, F.E. a Wiley Interscience Publication, John Wiley and Sons, New York, 3rd revised edition, 2A, page 2291
[2] Sokal, J. et al. (1980): Pol. J. Pharmacol. Pharm. 32, 223 - 229
[3] Oettel, H. (1958): Unveröffentlichte Untersuchung der BASF Aktiengesellschaft, Abteilung Toxikologie
[4] Gelbke, H.-P. (1978): Unveröffentlichte Untersuchung der BASF Aktiengesellschaft, Abteilung Toxikologie
[5] Waegemaekers, Th.H. und van der Walle, H.B. (1983): Contact Dermatitis 9, 372 - 376
[6] Parker, D. und Turk, J.L. (1983): Contact Dermatitis 9, 55 - 60
[7] Hunter, C.G. et al. (1966): British Journal Industrial Medicine 23, 137 - 141
[8] Gage, J.C. (1970): British Journal Industrial Medicine 27, 1 - 18
[9] Tedder, Yu.R. et al. (1967): Mater. Nanch.-Prakt. Konf. Molodyleh Gig. Sanit. Krachei, 11th, 226 - 229; zitiert aus: Chemical Abstract 72, 29.913 X
 |
weiter . |
(Stand: 20.08.2018)
Alle vollständigen Texte in der aktuellen Fassung im Jahresabonnement
Nutzungsgebühr: ab 105.- € netto
(derzeit ca. 7200 Titel s.Übersicht - keine Unterteilung in Fachbereiche)
Die Zugangskennung wird kurzfristig übermittelt
? Fragen ?
Abonnentenzugang/Volltextversion