

umwelt-online: Verordnung (EU) Nr. 142/2011 zur Durchführung der VO (EG) Nr. 1069/2009 mit Hygienevorschriften für nicht für den menschlichen Verzehr bestimmte tierische Nebenprodukte sowie zur Durchführung der RL 97/78/EG hinsichtlich bestimmter gemäß der genannten RL von Veterinärkontrollen an der Grenze befreiter Proben und Waren (3)
 |
zurück |  |
Kapitel II
Anforderungen an bestimmte organische Düngemittel und Bodenverbesserungsmittel
Abschnitt 113
Herstellungsbedingungen
1. Organische Düngemittel und Bodenverbesserungsmittel, ausgenommen Gülle, Magen- und Darminhalt, Kompost, Milch, Erzeugnisse auf Milchbasis, aus Milch gewonnene Erzeugnisse, Kolostrum, Kolostrumerzeugnisse und Fermentationsrückstände aus der Umwandlung von tierischen Nebenprodukten oder Folgeprodukten in Biogas sind wie folgt herzustellen:
2. Organische Düngemittel und Bodenverbesserungsmittel, die aus Fleisch- und Knochenmehl aus Material der Kategorie 2 oder aus verarbeitetem tierischen Protein bestehen oder aus diesem gewonnen wurden, müssen in einem registrierten Betrieb bzw. einer registrierten Anlage mit einem ausreichenden Mindestanteil eines Bestandteils gemischt werden, der von der zuständigen Behörde des Mitgliedstaats, in dem das Erzeugnis auf landwirtschaftliche Flächen ausgebracht werden soll, zu genehmigen ist, um zu verhindern, dass die Mischung anschließend zu Fütterungszwecken verwendet wird.
3. Die zuständige Behörde genehmigt den in Nummer 2 genannten Bestandteil unter folgenden Bedingungen:
Die zuständige Behörde macht der Kommission und anderen Mitgliedstaaten die Liste der zugelassenen Bestandteile auf Verlangen zugänglich.
4. Die Anforderungen gemäß Nummer 2 gelten jedoch nicht für
5. Die Hersteller von organischen Düngemitteln und Bodenverbesserungsmitteln müssen sicherstellen, dass vor dem Inverkehrbringen eine Abtötung von Krankheitserregern wie folgt vorgenommen wird:
Abschnitt 2
Lagerung und Beförderung
Nach der Verarbeitung bzw. Umwandlung sind organische Düngemittel und Bodenverbesserungsmittel wie folgt ordnungsgemäß zu lagern und zu befördern:
Abschnitt 3 15
Anforderungen an die Zulassung von Betrieben oder Anlagen
Um eine Zulassung gemäß Artikel 24 Absatz 1 Buchstabe f der Verordnung (EG) Nr. 1069/2009 zu erlangen, müssen die Betreiber sicherstellen, dass die Betriebe oder Anlagen, in denen die in Abschnitt 1 Nummer 1 genannten Tätigkeiten durchgeführt werden, den Anforderungen nach Artikel 8 der genannten Verordnung entsprechen und
| Zwischenprodukte | Anhang XII15 |
Gemäß Artikel 34 Absatz 2 der Verordnung (EG) Nr. 1069/2009 gelten für die Einfuhr von Zwischenprodukten in die Union und ihre Durchfuhr durch die Union die nachstehenden Bedingungen.
1. Die Einfuhr und Durchfuhr von Zwischenprodukten wird genehmigt, wenn folgende Anforderungen erfüllt sind:
2. Ein Betrieb bzw. eine Anlage kann von der zuständigen Behörde eines Drittlandes gemäß Nummer 1 Buchstabe e registriert oder zugelassen werden, sofern
3. Die in die Union eingeführten Zwischenprodukte werden gemäß Artikel 4 der Richtlinie 97/78/EG an der Grenzkontrollstelle kontrolliert und von dort auf direktem Wege entweder
4. Zwischenprodukte auf der Durchfuhr durch die Union werden gemäß Artikel 11 der Richtlinie 97/78/EG befördert.
5. Der amtliche Tierarzt/Die amtliche Tierärztin der betreffenden Grenzkontrollstelle informiert die für den Betrieb bzw. die Anlage am Bestimmungsort der Sendung zuständige Behörde über das TRACES-System.
6. Der Betreiber oder Eigentümer des Bestimmungsbetriebs bzw. der Bestimmungsanlage oder sein Vertreter führt Aufzeichnungen gemäß Artikel 22 der Verordnung (EG) Nr. 1069/2009 und stellt der zuständigen Behörde auf Anfrage die erforderlichen Angaben über Einkauf, Verkauf, Verwendung, Lagerhaltung und Beseitigung von überschüssigen Zwischenprodukten für die Überprüfung der Einhaltung der vorliegenden Verordnung zur Verfügung.
7. Die zuständige Behörde stellt gemäß der Richtlinie 97/78/EG sicher, dass die Sendungen mit Zwischenprodukten von dem Mitgliedstaat, in dem die Kontrolle an der Grenzkontrollstelle durchzuführen ist, zum Bestimmungsbetrieb gemäß Nummer 3 oder - im Fall der Durchfuhr - zur Ausgangsgrenzkontrollstelle verbracht werden.
8. Die zuständige Behörde führt regelmäßig Dokumentenkontrollen durch, um die Mengen der eingeführten Zwischenprodukte einerseits und der gelagerten, verwendeten, versandten oder beseitigten Zwischenerzeugnisse andererseits abzugleichen und somit die Einhaltung dieser Verordnung zu überprüfen.
9. Bei Durchfuhrsendungen mit Zwischenprodukten arbeiten die für die Einfuhr- bzw. Ausfuhrgrenzkontrollstelle zuständigen Behörden gegebenenfalls zusammen, um effektive Kontrollen und die Rückverfolgbarkeit solcher Sendungen zu gewährleisten.
| Heimtierfutter und bestimmte andere Folgeprodukte | Anhang XIII20 |
Kapitel I
Allgemeine Anforderungen
Heimtierfutterbetriebe und Betriebe bzw. Anlagen zur Herstellung von Folgeprodukten gemäß diesem Anhang müssen über geeignete Einrichtungen für folgende Zwecke verfügen:
Kapitel II
Spezielle Anforderungen an Heimtierfutter, einschließlich Kauspielzeug20
1. Rohes Heimtierfutter
Betreiber dürfen rohes Heimtierfutter ausschließlich aus Material der Kategorie 3 gemäß Artikel 10 Buchstabe a und Artikel 10 Buchstabe b Ziffern i und ii der Verordnung (EG) Nr. 1069/2009 herstellen.
Rohes Heimtierfutter muss in neuen, lecksicheren Verpackungen verpackt werden.
Es sind alle erforderlichen Vorkehrungen zu treffen, um sicherzustellen, dass das Erzeugnis auf allen Stufen seiner Herstellung und bis zur Abgabe im Einzelhandel vor Kontamination geschützt ist.
2. Rohmaterial für verarbeitetes Heimtierfutter und für Kauspielzeug
Betreiber dürfen verarbeitetes Heimtierfutter Kauspielzeug ausschließlich aus folgendem Material herstellen:
3. Verarbeitetes Heimtierfutter
Nach der Herstellung sind alle erforderlichen Vorkehrungen zu treffen, um eine Kontamination des verarbeiteten Heimtierfutters zu vermeiden.
Das verarbeitete Heimtierfutter ist in neuen Verpackungen zu verpacken.
4. Kauspielzeug muss einer Behandlung unterzogen werden, die gewährleistet, dass Krankheitserreger, einschließlich Salmonellen, wirksam abgetötet werden.
Nach der Behandlung sind alle erforderlichen Vorkehrungen zu treffen, um eine Kontamination des Kauspielzeugs zu vermeiden.
Das Kauspielzeug ist in neuen Verpackungen zu verpacken.
5. Von Kauspielzeug und von verarbeitetem Heimtierfutter, ausgenommen Heimtierfutter in Dosen und gemäß Nummer 3 Buchstabe b Ziffer v verarbeitetes Heimtierfutter, müssen während der Herstellung und/oder der Lagerung (vor dem Versand) Zufallsstichproben entnommen werden, damit nachgeprüft werden kann, ob folgende Normen erfüllt sind:
Salmonellen: kein Befund in 25 g, n = 5, c = 0, m = 0, M = 0,
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 in 1 g,
wobei
n = Anzahl der zu untersuchenden Proben,
m = Schwellenwert für die Keimzahl; das Ergebnis gilt als zufriedenstellend, wenn die Keimzahl in allen Proben m nicht überschreitet,
M = Höchstwert für die Keimzahl; das Ergebnis gilt als nicht zufriedenstellend, wenn die Keimzahl in einer oder mehreren Proben größer oder gleich M ist, und
c = Anzahl der Proben, bei denen die Keimzahl zwischen m und M liegen kann, wobei die Probe noch als zulässig gilt, wenn die Keimzahl in den anderen Proben m oder weniger beträgt.
6. Von rohem Heimtierfutter müssen während der Herstellung und/oder der Lagerung (vor dem Versand) Zufallsstichproben entnommen werden, damit nachgeprüft werden kann, ob folgende Normen erfüllt sind:
Salmonellen: kein Befund in 25 g, n = 5, c = 0, m = 0, M = 0,
Das Produktionsverfahren für rohes Heimtierfutter muss folgendes Prozesshygienekriterium erfüllen:
Enterobakterien: n = 5, c = 2, m = 500 in 1 g, M = 5.000 in 1 g.
Dabei ist
n = Anzahl der zu untersuchenden Proben;
m = Schwellenwert für die Keimzahl; das Ergebnis gilt als zufriedenstellend, wenn die Keimzahl in allen Proben m nicht überschreitet,
M = Höchstwert für die Keimzahl; das Ergebnis gilt als nicht zufriedenstellend, wenn die Keimzahl in einer oder mehreren Proben größer oder gleich M ist, und
c = Anzahl der Proben, bei denen die Keimzahl zwischen m und M liegen kann, wobei die Probe noch als zulässig gilt, wenn die Keimzahl in den anderen Proben m oder weniger beträgt.
Unternehmer sollten im Rahmen ihrer auf dem System der Gefahrenanalyse und kritischen Kontrollpunkte (HACCP-Grundsätze) basierenden Verfahren die erforderlichen Maßnahmen ergreifen, um die ihrer Kontrolle unterliegende Lieferung, Handhabung und Verarbeitung von Rohstoffen und Heimtiernahrung so durchzuführen, dass die oben genannten Sicherheitsnormen und Prozesshygienekriterien eingehalten werden. Werden die Sicherheitsnormen und Prozesshygienekriterien nicht eingehalten, führt der Unternehmer verhältnismäßige Abhilfemaßnahmen gemäß dem im einleitenden Satz von Artikel 29 Absatz 1 der Verordnung (EG) Nr. 1069/2009 und den auf HACCP-Grundsätzen beruhenden Verfahren durch, die in Artikel 29 Absatz 2 Buchstaben e und f dieser Verordnung erläutert werden.
Die Nichteinhaltung und, sofern ermittelt, ihre Ursache, die durchgeführten Abhilfemaßnahmen und die Ergebnisse der Kontrollmaßnahmen sind der zuständigen Behörde zu melden. Ist die zuständige Behörde nicht davon überzeugt, dass die erforderlichen Korrekturmaßnahmen getroffen wurden, kann sie dem Betreiber zusätzliche Maßnahmen auferlegen, darunter Kennzeichnung für die Handhabung, und die mikrobiologische Untersuchung weiterer Proben durch den Betreiber verlangen.
7. Endpunkt für verarbeitetes Heimtierfutter und für Kauspielzeug
Folgende Erzeugnisse dürfen gemäß dieser Verordnung ohne Einschränkung in Verkehr gebracht werden:
Kapitel III
Spezielle Anforderungen an geschmacksverstärkende Fleischextrakte zur Herstellung von Heimtierfutter
1. Betreiber dürfen zur Herstellung flüssiger oder dehydrierter Folgeprodukte, die zur Steigerung der Schmackhaftigkeit von Heimtierfutter bestimmt sind, ausschließlich tierische Nebenprodukte verwenden, die gemäß Kapitel II Nummer 2 als Rohmaterial für verarbeitetes Tierfutter und für Kauspielzeug verwendet werden dürfen.
2. Geschmacksverstärkende Fleischextrakte müssen nach einer Methode und nach Parametern verarbeitet worden sein, die gewährleisten, dass das Produkt den mikrobiologischen Normen gemäß Kapitel II Nummer 5 dieses Anhangs entspricht. Nach der Behandlung sind alle erforderlichen Maßnahmen zu treffen, um eine erneute Kontamination des Produkts zu verhindern.
3. Das Endprodukt muss
Kapitel IV
Spezielle Anforderungen an Blut und Blutprodukte von Equiden
Blut und Blutprodukte von Equiden für andere Zwecke als zur Verwendung in Futtermitteln dürfen unter folgenden Bedingungen in Verkehr gebracht werden:
1. Blut darf für solche Zwecke in Verkehr gebracht werden, wenn es
2. Blutprodukte dürfen für solche Zwecke in Verkehr gebracht werden, wenn
3. Blut und Blutprodukte von Equiden müssen in verplombte, undurchlässige Behälter verpackt werden, die im Fall von Blut von Equiden mit der Zulassungsnummer des Schlachthofs oder der Entnahmeeinrichtung gemäß Nummer 1 Buchstabe b zu versehen sind.
Kapitel V
Spezielle Anforderungen an Häute und Felle von Huftieren und daraus gewonnene Folgeprodukte
A. Betriebe und Anlagen
Die zuständige Behörde kann Betrieben, die Häute und Felle, einschließlich Kalkhäute, handhaben, die Genehmigung erteilen, Beschneideabfälle und Spalt dieser Häute und Felle zur Herstellung von Gelatine für die Tierernährung sowie von organischen Düngemitteln oder Bodenverbesserungsmitteln zu liefern, sofern folgende Bedingungen erfüllt sind:
B. Inverkehrbringen von tierischen Nebenprodukten und Folgeprodukten
1. Unbehandelte Häute und Felle dürfen in Verkehr gebracht werden, wenn die tierseuchenrechtlichen Vorschriften für frisches Fleisch gemäß der Richtlinie 2002/99/EG erfüllt sind.
2. Behandelte Häute und Felle dürfen in Verkehr gebracht werden, wenn
C. Endpunkt für Häute und Felle
1. Häute und Felle von Huftieren, die gemäß der Entscheidung eines Betreibers für andere Zwecke als zum menschlichen Verzehr bestimmt sind und den Anforderungen der Verordnung (EG) Nr. 853/2004 an Rohmaterial für Gelatine oder Kollagen entsprechen, die zur Verwendung in Lebensmitteln bestimmt sind, dürfen gemäß der vorliegenden Verordnung ohne Einschränkung in Verkehr gebracht werden.
2. Folgende behandelte Häute und Felle dürfen gemäß dieser Verordnung ohne Einschränkung in Verkehr gebracht werden:
3. Abweichend von Abschnitt C Nummer 2 kann die zuständige Behörde vorschreiben, dass Sendungen mit behandelten Häuten und Fellen gemäß Nummer 2 Buchstaben c und d ein Handelspapier beiliegen muss, das dem Muster in Anhang VIII Kapitel III Nummer 6 entspricht, wenn diese an Betriebe bzw. Anlagen geliefert werden, die Heimtierfutter, organische Düngemittel oder Bodenverbesserungsmittel herstellen oder solches Material in Biogas umwandeln.
Kapitel VI13 20
Spezielle Anforderungen an Jagdtrophäen und andere Tierpräparate
A. Die Bestimmungen dieses Kapitels berühren nicht die Maßnahmen zum Schutz wildlebender Tierarten gemäß der Verordnung (EG) Nr. 338/97.
B. Herkunftssicherung
Jagdtrophäen und andere Tierpräparate, zu deren Herstellung die tierischen Nebenprodukte einer Behandlung unterzogen wurden oder in einem Zustand präsentiert werden, der keinerlei Gesundheitsrisiken birgt, dürfen in Verkehr gebracht werden, sofern sie
C. Sichere Behandlung
1. Jagdtrophäen oder andere Tierpräparate, zu deren Herstellung die tierischen Nebenprodukte einer Behandlung unterzogen wurden oder in einem Zustand präsentiert werden, der keinerlei Gesundheitsrisiken birgt, dürfen in Verkehr gebracht werden, sofern
2. Andere als die in Abschnitt B und Abschnitt C Nummer 1 genannten Jagdtrophäen und anderen Präparate, die von Tieren aus einem Gebiet stammen, das wegen Ausbruchs schwerer übertragbarer Krankheiten, für die Tiere der betreffenden Arten empfänglich sind, Beschränkungen unterliegt, dürfen unter folgenden Bedingungen in Verkehr gebracht werden:
Kapitel VII12
Spezielle Anforderungen an Wolle, Haare, Schweinsborsten, Federn, Federteile und Daunen
A. Rohmaterial
1. Unbehandelte Wolle, unbehandelte Haare, unbehandelte Schweinsborsten sowie unbehandelte Federn, Federteile und Daunen sind gemäß Artikel 10 Buchstabe b Ziffern iii, iv und v sowie Artikel 10 Buchstaben h und n der Verordnung (EG) Nr. 1069/2009 als Material der Kategorie 3 einzustufen.
Sie müssen fest und trocken verpackt sein.
Im Fall von unbearbeiteten Federn, Federteilen und Daunen, die unmittelbar vom Schlachthof zur Verarbeitungsanlage verbracht werden, kann die zuständige Behörde jedoch eine Ausnahme von der Anforderung, dass das Material trocken befördert werden muss, gewähren, sofern
2. Verbringungen von Schweinsborsten und von Wolle und Haaren von Schweinen aus Regionen, in denen die afrikanische Schweinepest endemisch ist, sind verboten, es sei denn, die Schweinsborsten und die Wolle und Haare von Schweinen wurden
3. Die Bestimmungen gemäß Nummer 1 gelten nicht für Zierfedern oder Federn, die
B. Endpunkt für Wolle und Haare
Wolle und Haare, die einer Fabrikwäsche unterzogen oder mittels einer anderen Methode behandelt wurden, durch die gewährleistet ist, dass keine unannehmbaren Risiken verbleiben, dürfen gemäß dieser Verordnung ohne Einschränkung in Verkehr gebracht werden.
Die Mitgliedstaaten können gemäß der vorliegenden Verordnung das Inverkehrbringen unbehandelter Wolle und unbehandelter Haare aus Betrieben bzw. Anlagen, die gemäß Artikel 23 der Verordnung (EG) Nr. 1069/2009 registriert oder gemäß Artikel 24 Absatz 1 Ziffer i der genannten Verordnung zugelassen sind, in ihrem Hoheitsgebiet ohne Einschränkung genehmigen, wenn sie sich vergewissert haben, dass von der Wolle bzw. den Haaren keine unannehmbaren Risiken für die Gesundheit von Mensch und Tier ausgehen.
Wolle und Haare von anderen Tieren als Schweinen dürfen gemäß der vorliegenden Verordnung ohne Einschränkung in Verkehr gebracht werden, wenn sie
C. Endpunkt für Federn und Daunen
Federn, Federteile und Daunen, die einer Fabrikwäsche unterzogen und mindestens 30 Minuten lang mit heißem Dampf bei einer Temperatur von 100 °C behandelt wurden, dürfen gemäß dieser Verordnung ohne Einschränkung in Verkehr gebracht werden.
Kapitel VIII
Spezielle Anforderungen an Pelze
Endpunkt
Pelze, die zwei Tage lang bei einer Umgebungstemperatur von 18 °C und einer Luftfeuchtigkeit von 55 % getrocknet wurden, dürfen gemäß dieser Verordnung ohne Einschränkung in Verkehr gebracht werden.
Kapitel IX
Spezielle Anforderungen an Imkerei-Nebenerzeugnisse
Ausschließlich zur Verwendung in der Imkerei bestimmte Imkerei-Nebenerzeugnisse müssen folgende Bedingungen erfüllen:
1. Sie dürfen nicht aus einem Gebiet stammen, das wegen Ausbruchs einer der nachstehenden Krankheiten gesperrt ist:
2. müssen die Anforderungen in Artikel 8 Buchstabe a der Richtlinie 92/65/EWG erfüllen.
Kapitel X
Spezielle Anforderungen an ausgeschmolzene Fette aus Material der Kategorien 1 oder 2 für die Fettverarbeitung
1. Ausgeschmolzene Fette aus Material der Kategorien 1 oder 2, die zur Fettverarbeitung bestimmt sind, müssen nach einer der Verarbeitungsmethoden 1 bis 5 gemäß Anhang IV Kapitel III hergestellt werden.
2. Ausgeschmolzene Wiederkäuerfette sind so zu reinigen, dass der Rest an unlöslichen Unreinheiten insgesamt 0,15 Gew.- % nicht überschreitet.
Kapitel XI
Spezielle Anforderungen an Fettderivate13 20
1. Zur Gewinnung von Fettderivaten von ausgeschmolzenen Fetten aus Material der Kategorien 1 und 2 können folgende Verfahren eingesetzt werden:
2. Gemäß diesem Kapitel hergestellte Fettderivate dürfen nur wie folgt in Verkehr gebracht werden:
3. Endpunkt für aus ausgeschmolzenen Fetten hergestellte Produkte:
Fettderivate, die gemäß Nummer 1 verarbeitet wurden, dürfen gemäß dieser Verordnung ohne Einschränkungen für die in Nummer 2 genannten Verwendungen in Verkehr gebracht werden.
Kapitel XII
Spezielle Anforderungen an Hörner und Hornprodukte (außer Hornmehl) sowie Hufe und Hufprodukte (außer Hufmehl), die zur Herstellung von organischen Düngemitteln oder Bodenverbesserungsmitteln bestimmt sind
Hörner und Hornprodukte (außer Hornmehl) sowie Hufe und Hufprodukte (außer Hufmehl), die zur Herstellung von organischen Düngemitteln oder Bodenverbesserungsmitteln bestimmt sind, dürfen unter folgenden Bedingungen in Verkehr gebracht werden:
Kapitel XIII
Spezifische Anforderungen an Fischöl zur Herstellung von Arzneimitteln
Endpunkt für Fischöl zur Herstellung von Arzneimitteln
Fischöl, das aus Material gemäß Anhang X Kapitel II Abschnitt 3 Buchstabe a Nummer 2 gewonnen und mit einer NaOH-Lösung bei einer Temperatur von mindestens 80 °C entsäuert sowie anschließend durch Destillation bei einer Temperatur von mindestens 200 °C gereinigt wurde, darf ohne Einschränkungen gemäß der vorliegenden Verordnung für die Herstellung von Arzneimitteln in Verkehr gebracht werden.
| Einfuhr, Ausfuhr und Durchfuhr | Anhang XIV20 20a |
Kapitel I
Spezielle Anforderungen an die Einfuhr in die und die Durchfuhr durch die Union von Material der Kategorie 3 und von Folgeprodukten zur Verwendung in der Futtermittelkette ausser als Heimtierfutter oder als Futter für Pelztiere 13 17
Gemäß Artikel 41 Absatz 1 Buchstabe a und Artikel 41 Absatz 3 der Verordnung (EG) Nr. 1069/2009 gelten für eingeführte Sendungen mit Material der Kategorie 3 und dessen Folgeprodukten, die zur Verwendung in der Futtermittelkette - außer als Heimtierfutter oder als Futter für Pelztiere - bestimmt sind, sowie für Sendungen mit solchem Material bzw. solchen Produkten auf der Durchfuhr folgende Anforderungen:
Tabelle 115 17 19
| Nr. | Produkt | Rohmaterial (Verweis auf die Bestimmungen der Verordnung (EG) Nr. 1069/2009) | Einfuhr- und Durchfuhrbedingungen | Listen der Drittländer | Bescheinigungen/Muster |
| 1 | Verarbeitetes tierisches Protein, einschließlich solches Protein enthaltende Mischungen und Produkte außer Heimtierfutter, und solches Protein enthaltende Mischfuttermittel gemäß Artikel 3 Absatz 2 Buchstabe h der Verordnung (EG) Nr. 767/2009 | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d, e, f, h, i, j, k, l und m | a) Das verarbeitete tierische Protein muss gemäß Anhang X Kapitel II Abschnitt 1 hergestellt worden sein, und
b) das verarbeitete tierische Protein muss die zusätzlichen Anforderungen gemäß Abschnitt 2 dieses Kapitels erfüllen. |
a) Im Fall von verarbeitetem tierischem Protein außer Fischmehl:
Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 b) Im Fall von Fischmehl: Drittländer gemäß Anhang II der Entscheidung 2006/766/EG |
a) Im Fall von verarbeitetem tierischem Protein, ausgenommen solches aus Nutzinsekten:
b) Im Fall von verarbeitetem tierischem Protein aus Nutzinsekten: Anhang XV Kapitel 1a |
| 2 | Blutprodukte als Futtermittel-Ausgangserzeugnisse | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a und Buchstabe b Ziffer i | Die Blutprodukte müssen gemäß Anhang X Kapitel II Abschnitt 2 und Anhang XIV Kapitel I Abschnitt 5 hergestellt worden sein. | a) Im Fall von Blutprodukten von Huftieren:
Drittländer bzw. Teile von Drittländern gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, aus denen alle Kategorien frischen Fleisches der betreffenden Tierarten eingeführt werden dürfen; b) Im Fall von Blutprodukten von anderen Tierarten: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 |
Anhang XV Kapitel 4 Buchstabe B |
| 3 | Ausgeschmolzene Fette und Fischöl |
a) Im Fall von ausgeschmolzenen Fetten außer Fischöl: Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d, e, f, g, h, i, j und k;
b) im Fall von Fischöl: Material der Kategorie 3 gemäß Artikel 10 Buchstaben e, f, i und j |
a) Die ausgeschmolzenen Fette und das Fischöl müssen gemäß Anhang X Kapitel II Abschnitt 3 hergestellt worden sein, und
b) das ausgeschmolzene Fett muss die zusätzlichen Anforderungen gemäß Abschnitt 3 dieses Kapitels erfüllen. |
a) Im Fall von ausgeschmolzenen Fetten außer Fischöl: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010; b) im Fall von Fischöl: Drittländer gemäß Anhang II der Entscheidung 2006/766/EG |
a) Im Fall von ausgeschmolzenen Fetten außer Fischöl:
Anhang XV Kapitel 10 Buchstabe A; b) im Fall von Fischöl: Anhang XV Kapitel 9 |
| 4 | Milch, Erzeugnisse auf Milchbasis oder aus Milch gewonnene Erzeugnisse, Kolostrum und Kolostrumerzeugnisse | a) Milch, Erzeugnisse auf Milchbasis:
Material der Kategorie 3 gemäß Artikel 10 Buchstaben e, f und h; b) Kolostrum, Kolostrumerzeugnisse: Material der Kategorie 3 von lebenden Tieren, die keine Anzeichen einer durch Kolostrum auf Mensch oder Tier übertrag- baren Krankheit aufwiesen |
Die Milch, die Erzeugnisse auf Milchbasis, das Kolostrum und die Kolostrumerzeugnisse müssen die Anforderungen gemäß Abschnitt 4 dieses Kapitels erfüllen. | a) Im Fall von Milch und Erzeugnissen auf Milchbasis:
zugelassene Drittländer gemäß Anhang I der Verordnung (EU) Nr. 605/2010; b) im Fall von Kolostrum und Kolostrumerzeugnissen: in Anhang I Spalte a der Verordnung (EU) Nr. 605/2010 als zugelassen aufgeführte Drittländer |
a) Im Fall von Milch, Erzeugnissen auf Milchbasis und aus Milch gewonnenen Erzeugnissen:
Anhang XV Kapitel 2 Buchstabe A; b) im Fall von Kolostrum und Kolostrumerzeugnissen: Anhang XV Kapitel 2 Buchstabe B |
| 5 | Gelatine und hydrolysiertes Protein | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, e, f, g, i und j, sowie im Fall von hydrolysiertem Protein: Material der Kategorie 3 gemäß Artikel 10 Buchstaben d, h und k | Die Gelatine und das hydrolysierte Protein müssen gemäß Anhang X Kapitel II Abschnitt 5 hergestellt worden sein. |
|
|
| 6 | Dicalciumphosphat | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d, e, f, g, h, i, j und k | Das Dicalciumphosphat muss gemäß Anhang X Kapitel II Abschnitt 6 hergestellt worden sein. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und folgende Länder:
Südkorea (KR), Malaysia (MY), Pakistan (PK), Taiwan (TW) |
Anhang XV Kapitel 12 |
| 7 | Tricalciumphosphat | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d, e, f, g, h, i und k | Das Tricalciumphosphat muss gemäß Anhang X Kapitel II Abschnitt 7 hergestellt worden sein. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und folgende Länder:
Südkorea (KR), Malaysia (MY), Pakistan (PK), Taiwan (TW) |
Anhang XV Kapitel 12 |
| 8 | Kollagen | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, e, f, g, i und j | Das Kollagen muss gemäß Anhang X Kapitel II Abschnitt 8 hergestellt worden sein. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und folgende Länder:
Südkorea (KR), Malaysia (MY), Pakistan (PK), Taiwan (TW) |
Anhang XV Kapitel 11 |
| 9 | Eiprodukte | Material der Kategorie 3 gemäß Artikel 10 Buchstabe e, Buchstabe f und Buchstabe k Ziffer ii | Die Eiprodukte müssen gemäß Anhang X Kapitel II Abschnitt 9 hergestellt worden sein. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und in Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008 aufgeführte Drittländer bzw. Teile von Drittländern, aus denen die Mitgliedstaaten die Einfuhr von frischem Geflügelfleisch, Eiern und Eiprodukten zulassen | Anhang XV Kapitel 15 |
Abschnitt 217
Einfuhr von verarbeitetem tierischem Protein einschließlich Mischungen und Produkten außer Heimtierfutter, das solches Protein enthält, mit Ausnahme von Mischfuttermitteln gemäß Artikel 3 Absatz 2 Buchstabe h der Verordnung (EG) Nr. 767/2009.
1. Bevor die Sendungen in den freien Verkehr innerhalb der Union überführt werden, muss die zuständige Behörde an der Grenzkontrollstelle von dem verarbeiteten tierischen Protein aus eingeführten Sendungen Proben nehmen, um sicherzustellen, dass die allgemeinen Anforderungen von Anhang X Kapitel I erfüllt sind.
Die zuständige Behörde muss
2. Abweichend von Nummer 1 darf sich jedoch die zuständige Behörde der Grenzkontrollstelle, wenn sechs aufeinanderfolgende Untersuchungen von Massengutsendungen aus einem bestimmten Drittland negativ ausgefallen sind, bei anschließenden Massengutsendungen aus diesem Drittland auf Stichprobenuntersuchungen beschränken.
Hat eine dieser Stichprobenuntersuchungen einen Positivbefund ergeben, muss die zuständige Behörde, die die Beprobung durchführt, die zuständige Behörde des Herkunftsdrittlandes entsprechend unterrichten, damit diese geeignete Abhilfemaßnahmen treffen kann.
Die zuständige Behörde des Herkunftsdrittlandes muss diese Maßnahmen der für die Beprobung zuständigen Behörde mitteilen.
Im Fall eines weiteren Positivbefunds bei Erzeugnissen derselben Herkunft muss die zuständige Behörde der Grenzkontrollstelle von allen weiteren Sendungen derselben Herkunft so lang Proben nehmen, bis erneut sechs aufeinanderfolgende Untersuchungen negativ ausfallen.
3. Die zuständigen Behörden müssen über die Probenbefunde sämtlicher Sendungen, von denen Proben genommen wurden, Aufzeichnungen führen und diese mindestens drei Jahre lang aufbewahren.
4. Wenn eine in die Union eingeführte Sendung positiv auf Salmonella getestet wird oder die mikrobiologischen Normen für Enterobacteriaceae gemäß Anhang X Kapitel I nicht erfüllt, ist sie entweder
5. Verarbeitetes tierisches Protein aus Nutzinsekten darf in die Union eingeführt werden, sofern es gemäß folgenden Bedingungen hergestellt wurde:
Abschnitt 3
Einfuhr von ausgeschmolzenen Fetten
Für die Einfuhr von ausgeschmolzenen Fetten gelten folgende Anforderungen: Das ausgeschmolzene Fett
Die Parameter der kritischen Kontrollpunkte sind vom Betreiber aufzuzeichnen und zu verwahren, damit der Eigentümer, der Betreiber oder deren Vertreter und, falls nötig, die zuständige Behörde den Betriebsablauf überwachen können. Aufzuzeichnen sind unter anderem Partikelgröße, kritische Temperatur und gegebenenfalls Absolutzeit, Druckprofil, Vorschubgeschwindigkeit des Rohmaterials und Fettrecyclingrate.
Abschnitt 4
Einfuhr von Milch, Erzeugnissen auf Milchbasis, aus Milch gewonnenen Erzeugnissen, Kolostrum und Kolostrumerzeugnissen
A. Für die Einfuhr von Milch, Erzeugnissen auf Milchbasis, aus Milch gewonnenen Erzeugnissen, Kolostrum und Kolostrumerzeugnissen gelten folgende Anforderungen:
1. Milch, Erzeugnisse auf Milchbasis und aus Milch gewonnene Erzeugnisse
- wurden zumindest einer der Behandlungen gemäß Anhang X Kapitel II Abschnitt 4 Teil I Nummern 1.1, 1.2 und 1.3 sowie Abschnitt B Nummer 1.4 Buchstabe a unterzogen,
- erfüllen die Bedingungen gemäß Anhang X Kapitel II Abschnitt 4 Teil I Abschnitt B Nummern 2 und 4 sowie - im Fall von Molke - Abschnitt B Nummer 3.
2. Abweichend von Anhang X Kapitel II Abschnitt 4 Teil I Abschnitt B Nummer 1.4 dürfen Milch, Erzeugnisse auf Milchbasis und aus Milch gewonnene Erzeugnisse aus Drittländern eingeführt werden, die gemäß Spalte a in Anhang I der Verordnung (EU) Nr. 605/2010 zugelassen sind, sofern die Milch, Erzeugnisse auf Milchbasis bzw. aus Milch gewonnenen Erzeugnisse einer einmaligen HTST unterzogen und
- frühestens 21 Tage nach ihrer Herstellung versandt wurden, wobei während dieses Zeitraums im Ausfuhrdrittland kein Fall von Maul- und Klauenseuche aufgetreten ist, oder
- frühestens 21 Tage nach ihrer Herstellung an einer Grenzkontrollstelle des Eingangs in die Union gestellt wurden, wobei während dieses Zeitraums im Ausfuhrdrittland kein Fall von Maul- und Klauenseuche aufgetreten ist.
B. Für die Einfuhr von Kolostrum und Kolostrumerzeugnissen gelten folgende Anforderungen:
1. Das Material wurde einer einmaligen HTST unterzogen und
- frühestens 21 Tage nach seiner Herstellung versandt, wobei während dieses Zeitraums im Ausfuhrdrittland kein Fall von Maul- und Klauenseuche aufgetreten ist, oder
- frühestens 21 Tage nach seiner Herstellung an einer Grenzkontrollstelle des Eingangs in die Union gestellt, wobei während dieses Zeitraums im Ausfuhrdrittland kein Fall von Maul- und Klauenseuche aufgetreten ist.
2. Das Material wurde von Rindern gewonnen, die regelmäßigen Veterinärkontrollen unterworfen werden, damit gewährleistet ist, dass die Tiere aus Betrieben stammen, in denen alle Rinderbestände
- entweder amtlich anerkannt tuberkulosefrei und amtlich anerkannt brucellosefrei gemäß Artikel 2 Absatz 2 Buchstaben d und f der Richtlinie 64/432/EWG sind oder nach nationalem Recht des Herkunftsdrittlandes des Kolostrums keinen Beschränkungen im Hinblick auf die Tilgung von Tuberkulose und Brucellose unterliegen, und
- entweder amtlich anerkannt leukosefrei gemäß Artikel 2 Absatz 2 Buchstabe j der Richtlinie 64/432/EWG sind oder einem amtlichen System zur Bekämpfung der enzootischen Rinderleukose unterliegen, wobei diese Krankheit in den letzten zwei Jahren im fraglichen Bestand weder klinisch noch in Laboruntersuchungen nachgewiesen wurde.
3. Nach Abschluss der Verarbeitung wurden alle erforderlichen Vorkehrungen getroffen, um eine Kontamination des Kolostrums oder der Kolostrumerzeugnisse zu vermeiden.
4. Das Enderzeugnis muss mit dem Hinweis versehen sein, dass es Material der Kategorie 3 enthält und nicht für den menschlichen Verzehr bestimmt ist, und es wurde
- in neue Behälter abgefüllt oder
- als Massengut in Containern oder sonstigen Transportmitteln befördert, die vor ihrer Verwendung gründlich gereinigt und desinfiziert wurden.
Abschnitt 515
Einfuhr von Blutprodukten zur Verfütterung an Nutztiere
Die folgenden Anforderungen gelten für die Einfuhr von Blutprodukten von Schweinen, einschließlich sprühgetrocknetem Blut und Blutplasma, die zur Verfütterung an Schweine bestimmt sind:
Diese Folgeprodukte
Kapitel II
Spezielle Anforderungen an die Einfuhr in die und die Durchfuhr durch die Union von tierischen Nebenprodukten und Folgeprodukten zur Verwendung ausserhalb der Futtermittelkette für Nutztiere ausser Pelztieren 13
Abschnitt 1
Spezielle Anforderungen
Gemäß Artikel 41 Absatz 1 Buchstabe a, Artikel 41 Absatz 2 Buchstabe c und Artikel 41 Absatz 3 der Verordnung (EG) Nr. 1069/2009 gelten für eingeführte Sendungen mit tierischen Nebenprodukten und Folgeprodukten, die zur Verwendung außerhalb der Futtermittelkette für Nutztiere bestimmt sind, sowie für Sendungen mit solchen Produkten auf der Durchfuhr folgende spezielle Anforderungen:
Tabelle 212 13 17 19 20
| Nr. | Produkt | Rohmaterial (Verweis auf die Bestimmungen der Verordnung (EG) Nr. 1069/2009) | Einfuhr- und Durchfuhrbedingungen | Listen der Drittländer | Bescheinigungen/Muster |
| 1 | Verarbeitete Gülle, aus dieser gewonnene Folgeprodukte und Guano von Fledermäusen | Material der Kategorie 2 gemäß Artikel 9 Buchstabe a | Verarbeitete Gülle, aus dieser gewonnene Folgeprodukte und Guano von Fledermäusen müssen gemäß Anhang XI Kapitel I Abschnitt 2 hergestellt worden sein. | Drittländer gemäß
|
Anhang XV Kapitel 17 |
| 2 | Blutprodukte, außer von Equiden, zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere | Material der Kategorie 1 gemäß Artikel 8 Buchstaben c und d sowie Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d und h | Die Blutprodukte müssen gemäß Abschnitt 2 hergestellt worden sein. | Folgende Drittländer:
a) im Fall unbehandelter Blutprodukte von Huftieren: Drittländer bzw. Teile von Drittländern gemäß An- hang II Teil 1 der Verordnung (EU) Nr. 206/2010, aus denen frisches Fleisch von domestizierten Huftierarten eingeführt werden darf, und zwar nur für den Zeitraum gemäß den Spalten 7 und 8 des genannten Teils, Japan; b) im Fall unbehandelter Blutprodukte von Geflügel und anderen Vogelarten: Drittländer bzw. Teile von Drittländern gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008, Japan; c) im Fall unbehandelter Blutprodukte von anderen Tieren: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 der Kommission, gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008 oder gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 119/2009, Japan; d) im Fall behandelter Blutprodukte von allen Tierarten: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 der Kommission, gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008 oder gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 119/2009, Japan |
a) Im Fall unbehandelter Blutprodukte:
Anhang XV Kapitel 4 Buchstabe C; b) im Fall behandelter Blutprodukte: Anhang XV Kapitel 4 Buchstabe D |
| 3 | Blut und Blutprodukte von Equiden | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, d und h | Das Blut und die Blutprodukte müssen die Anforderungen gemäß Abschnitt 3 erfüllen. | Folgende Drittländer:
|
Anhang XV Kapitel 4 Buchstabe A |
| 4 | Frische oder gefühlte Häute und Felle von Huftieren | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a und Buchstabe b Ziffer iii | Die Häute und Felle müssen die Anforderungen gemäß Abschnitt 4 Nummern 1 und 4 erfüllen. | Die Häute und Felle stammen aus einem Drittland bzw. im Fall einer Regionalisierung nach Unions- recht - einem Teil eines Drittlandes gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, aus dem die Mitgliedstaaten die Einfuhr frischen Fleisches derselben Tierart zulassen. | Anhang XV Kapitel 5 Buchstabe A |
| 5 | Behandelte Häute und Felle von Huftieren | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a, Buchstabe b Ziffern i und iii sowie Buchstabe n | Die Häute und Felle müssen die Anforderungen gemäß Abschnitt 4 Nummern 2, 3 und 4 erfüllen. |
a) Im Fall behandelter Häute und Felle von Huftieren:
Drittländer bzw. Teile von Drittländern gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010; b) im Fall behandelter Häute und Felle von Wiederkäuern, die zum Versand in die Europäische Union bestimmt sind und vor der Einfuhr 21 Tage getrennt gehalten wurden oder mindestens 21 Tage ohne Unterbrechung befördert werden: jedes Drittland |
a) Im Fall behandelter Häute und Felle von Huftieren, die nicht den Anforderungen gemäß Abschnitt 4 Nummer 2 entsprechen:
Anhang XV Kapitel 5 Buchstabe B; b) im Fall behandelter Häute und Felle von Wiederkäuern und Equiden, die zum Versand in die Europäische Union bestimmt sind und vor der Einfuhr 21 Tage getrennt gehalten wurden oder mindestens 21 Tage ohne Unterbrechung befördert werden: amtliche Erklärung gemäß Anhang XV Kapitel 5 Buchstabe C; c) im Fall behandelter Häute und Felle von Huftieren, die die Anforderungen gemäß Abschnitt 4 Nummer 2 erfüllen: keine Bescheinigung erforderlich |
| 6 | Jagdtrophäen und andere Tierpräparate | Material der Kategorie 2 gemäß Artikel 9 Buchstabe f, das von Wildtieren gewonnen wurde, bei denen kein Verdacht auf eine In- fektion mit einer auf Mensch oder Tier übertragbaren Krankheit be- steht, sowie Material der Kategorie 3 gemäß Artikel 10 Buchstabe a, Buchstabe b Ziffern i, iii und v sowie Buchstabe n | Die Jagdtrophäen und anderen Präparate müssen die Anforderungen gemäß Abschnitt 5 erfüllen. | a) Im Fall von Jagdtrophäen und anderen Präparaten gemäß Abschnitt 5 Nummer 2:
jedes Drittland; b) Im Fall von Jagdtrophäen und anderen Präparaten gemäß Abschnitt 5 Nummer 3:
|
a) Im Fall von Jagdtrophäen gemäß Abschnitt 5 Nummer 2: Anhang XV Kapitel 6 Buchstabe A;
b) im Fall von Jagdtrophäen gemäß Abschnitt 5 Nummer 3: Anhang XV Kapitel 6 Buchstabe B; c) im Fall von Jagdtrophäen gemäß Abschnitt 5 Nummer 1: keine Bescheinigung erforderlich |
| 7 | Schweineborsten | Material der Kategorie 3 gemäß Artikel 10 Buchstabe b Ziffer iv | Die Schweineborsten müssen von Schweinen gewonnen worden sein, die aus dem Herkunftsdrittland stammen und dort in einem Schlachthof geschlachtet wurden. | a) Im Fall unbearbeiteter Schweineborsten:
Drittländer bzw. - im Fall einer Regionalisierung - Teile von Drittländern gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, die in den letzten 12 Monaten vor dem Datum der Einfuhr frei von afrikanischer Schweinepest waren; b) im Fall bearbeiteter Schweineborsten: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, die in den letzten 12 Monaten vor dem Datum der Einfuhr möglicherweise nicht frei von afrikanischer Schweinepest waren. |
a) Falls in den letzten 12 Monaten kein Fall von afrikanischer Schweinepest aufgetreten ist:
Anhang XV Kapitel 7 Buchstabe A; b) falls in den letzten 12 Monaten mindestens ein Ausbruch von afrikanischer Schweinepest aufgetreten ist: Anhang XV Kapitel 7 Buchstabe B |
| 8 | Unbehandelte Wolle und unbehandelte Haare von anderen Tieren als Schweinen | Material der Kategorie 3 gemäß Artikel 10 Buchstaben h und n | (1) Trockene unbehandelte Wolle und trockene unbehandelte Haare müssen
(2) Die Wolle und die Haare gelten als Wolle und Haare gemäß Artikel 25 Absatz 2 Buchstabe e. |
(1) Jedes Drittland
(2) Drittland oder Gebiet eines Drittlandes,
|
(1) Für die Einfuhr unbehandelter Wolle und unbehandelter Haare ist keine Veterinärbescheinigung erforderlich. (2) Eine Erklärung des Einführers gemäß Anhang XV Kapitel 21 ist erforderlich. |
| 9 | Bearbeitete Federn, Federteile und Daunen | Material der Kategorie 3 gemäß Artikel 10 Buchstabe b Ziffer v so- wie Buchstaben h und n | Die bearbeiteten Federn bzw. Federteile müssen die Anforderungen gemäß Abschnitt 6 erfüllen. | Jedes Drittland | Für die Einfuhr bearbeiteter Federn, Federteile oder Daunen ist keine Veterinärbescheinigung erforderlich. |
| 10 | Imkerei-Nebenerzeugnisse | Material der Kategorie 3 gemäß Artikel 10 Buchstabe e | a) Im Fall anderer Imkerei-Nebenerzeugnisse als Bienenwachs in Wabenform, die zur Verwendung in der Imkerei bestimmt sind:
b) wurden im Fall von anderem Bienenwachs als Bienenwachs in Wabenform, das für andere Zwecke als die Verfütterung an Nutztiere bestimmt ist, vor der Einfuhr nach einer der Verarbeitungsmethoden 1 bis 5 oder nach der Verarbeitungsmethode 7 gemäß Anhang IV Kapitel III raffiniert oder verarbeitet. |
a) Im Fall von Imkerei-Nebenerzeugnissen zur Verwendung in der Imkerei:
Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und folgendes Land: Kamerun (CM); b) im Fall von Bienenwachs für andere Zwecke als die Verfütterung an Nutztiere: jedes Drittland |
a) Im Fall von Imkerei-Nebenerzeugnissen zur Verwendung in der Imkerei:
Anhang XV Kapitel 13; b) im Fall von Bienenwachs für andere Zwecke als die Verfütterung an Nutztiere: ein Handelspapier, in dem |
| 11 | Knochen und Knochenerzeugnisse (außer Knochenmehl), Hörner und Hornerzeugnisse (außer Hornmehl) sowie Hufe und Huferzeugnisse (außer Hufmehl), die nicht zur Verwendung als Futtermittel-Ausgangserzeugnisse, organische Düngemittel oder Bodenverbesserungsmittel bestimmt sind | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a, Buchstabe b Ziffern i und iii sowie Buchstaben e und h | Die Erzeugnisse müssen die Anforderungen gemäß Abschnitt 7 erfüllen. | Jedes Drittland | Den Erzeugnissen liegt Folgendes bei:
a) ein Handelspapier gemäß Abschnitt 7 Nummer 2 und b) eine Erklärung des Einführers gemäß Anhang XV Kapitel 16, die in mindestens einer der Amtssprachen des Mitgliedstaats der Einfuhr in die Union und in mindestens einer der Amtssprachen des Bestimmungsmitgliedstaats abgefasst sein muss. |
| 12 | Heimtierfutter und Kauspielzeug
Stand: VO (EU) 2020/207 |
a) Im Fall von verarbeitetem Heimtierfutter und von Kauspielzeug: Material gemäß Artikel 35 Buchstabe a Ziffern i und ii;
b) im Fall von rohem Heimtierfutter: Material gemäß Artikel 35 Buchstabe a Ziffer iii. |
Das Heimtierfutter und das Kauspielzeug müssen gemäß Anhang XIII Kapitel II hergestellt worden sein. | a) Im Fall von rohem Heimtierfutter: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 oder gemäß Anhang I der Verordnung (EG) Nr. 798/2008, aus denen die Mitgliedstaaten unter der Bedingung, dass nur Fleisch mit Knochen eingeführt wird, die Einfuhr von frischem Fleisch derselben Tierart zulassen; im Fall von Fischmaterial: Drittländer gemäß Anhang II der Entscheidung 2006/766/EG; b) im Fall von Kauspielzeug und anderem als rohem Heimtierfutter: (JP) Japan |
a) Im Fall von Heimtierfutter in Dosen: Anhang XV Kapitel 3 Buchstabe A;
b) im Fall von verarbeitetem Heimtierfutter außer Heimtierfutter in Dosen: Anhang XV Kapitel 3 Buchstabe B; c) im Fall von Kauspielzeug: Anhang XV Kapitel 3 Buchstabe C; d) im Fall von rohem Heimtierfutter: Anhang XV Kapitel 3 Buchstabe D. |
| 13 | Geschmacksverstärkende Fleischextrakte zur Herstellung von Heimtierfutter | Material gemäß Artikel 35 Buchstabe a | Die geschmacksverstärkenden Fleischextrakte müssen gemäß Anhang XIII Kapitel III hergestellt worden sein. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, aus denen die Mitgliedstaaten unter der Bedingung, dass nur Fleisch mit Knochen eingeführt wird, die Einfuhr von frischem Fleisch derselben Tierart zulassen;
im Fall geschmacksverstärkender Fleischextrakte aus Fischmaterial: Drittländer gemäß Anhang II der Entscheidung 2006/766/EG; im Fall geschmacksverstärkender Fleischextrakte aus Geflügelfleisch: Drittländer gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008, aus denen die Mitgliedstaaten die Einfuhr frischen Geflügelfleischs zulassen; im Fall geschmacksverstärkender Fleischextrakte aus Fleisch von bestimmten wildlebenden Landsäugetieren und Hasenartigen: Drittländer gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 119/2009, aus denen die Mitgliedstaaten die Einfuhr von frischem Fleisch derselben Tierart zulassen. |
Anhang XV Kapitel 3 Buchstabe E. |
| 14 | Tierische Nebenprodukte für die Herstellung von anderem als rohem Heimtierfutter und von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette | a) Material der Kategorie 3 gemäß Artikel 10 Buchstaben a bis m;
b) im Fall von Material zur Herstellung von Heimtierfutter: Material der Kategorie 1 gemäß Artikel 8 Buchstabe c; c) im Fall von Pelzen zur Herstellung von Folgeprodukten: Material der Kategorie 3 gemäß Artikel 10 Buchstaben |
Die Erzeugnisse bzw. Produkte müssen die Anforderungen gemäß Abschnitt 8 erfüllen. | a) Im Fall tierischer Nebenprodukte zur Herstellung von Heimtierfutter:
b) im Fall tierischer Nebenprodukte zur Herstellung von Pharmazeutika: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008 oder gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 119/2009 sowie folgende Drittländer: Japan (JP), Philippinen (PH), Taiwan (TW); c) im Fall tierischer Nebenprodukte für die Herstellung von Produkten zur Verwendung außerhalb der Futtermittelkette für Nutztiere, ausgenommen pharmazeutische Verwendungszwecke: Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010, aus denen frisches Fleisch der betreffenden Tierart eingeführt werden darf, gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 798/2008, gemäß Anhang I Teil 1 der Verordnung (EG) Nr. 119/2009 bzw. - im Fall von Material aus Fisch - Drittländer gemäß Anhang II der Entscheidung 2006/766/EG |
a) Im Fall tierischer Nebenprodukte zur Herstellung von verarbeitetem Heimtierfutter:
Anhang XV Kapitel 3 Buchstabe F; b) im Fall tierischer Nebenprodukte für die Herstellung von Produkten zur Verwendung außerhalb der Futtermittelkette für Nutztiere: Anhang XV Kapitel 8 |
| 15 | Tierische Nebenprodukte zur Verwendung als rohes Heimtierfutter | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a und Buchstabe b Ziffern i und ii | Die Produkte müssen die Anforderungen gemäß Abschnitt 8 erfüllen. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 oder gemäß Anhang I der Verordnung (EG) Nr. 798/2008, aus denen die Mitgliedstaaten unter der Bedingung, dass nur Fleisch mit Knochen eingeführt wird, die Einfuhr von frischem Fleisch derselben Tierart zulassen;
im Fall von Fischmaterial: |
Anhang XV Kapitel 3(D) |
| 16 | Tierische Nebenprodukte zur Verwendung in Futter für Pelztiere | Material der Kategorie 3 gemäß Artikel 10 Buchstabe a und Buchstaben a bis m | Die Produkte müssen die Anforderungen gemäß Abschnitt 8 erfüllen. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 der Kommission oder gemäß Anhang I der Verordnung (EG) Nr. 798/2008, aus denen die Mitgliedstaaten unter der Bedingung, dass nur Fleisch mit Knochen eingeführt wird, die Einfuhr von frischem Fleisch derselben Tierart zulassen;
im Fall von Fischmaterial: Drittländer gemäß Anhang II der Entscheidung 2006/766/EG |
Anhang XV Kapitel 3(D) |
| 17 | Ausgeschmolzene Fette für bestimmte Zwecke außerhalb der Futtermittelkette für Nutztiere |
|
Die ausgeschmolzenen Fette müssen die Anforderungen gemäß Abschnitt 9 erfüllen. | Drittländer gemäß Anhang II Teil 1 der Verordnung (EU) Nr. 206/2010 und im Fall von Fischmaterial Drittländer gemäß Anhang II der Entscheidung 2006/766/EG. | Anhang XV Kapitel 10 Buchstabe B. |
| 18 | Fettderivate | a) Im Fall von Fettderivaten zur Verwendung außerhalb der Futtermittelkette für Nutztiere:
Material der Kategorie 1 gemäß Artikel 8 Buchstaben b, c und d, Material der Kategorie 2 gemäß Artikel 9 Buchstaben c und d sowie Buchstabe f Ziffer i und Material der Kategorie 3 gemäß Artikel 10; b) im Fall von Fettderivaten zur Verwendung als Futter: Material der Kategorie 3 außer Material gemäß Artikel 10 Buchstaben n, o und p |
Die Fettderivate müssen die Anforderungen gemäß Abschnitt 10 erfüllen. | Jedes Drittland | a) Im Fall von Fettderivaten zur Verwendung außerhalb der Futtermittelkette für Nutztiere:
Anhang XV Kapitel 14(A); b) im Fall von Fettderivaten zur Verwendung als Futter: Anhang XV Kapitel 14(B) |
| 19 | Fotogelatine | Material der Kategorie 1 gemäß Artikel 8 Buchstabe b und Material der Kategorie 3 gemäß Artikel 10 | Die eingeführte Fotogelatine muss die Anforderungen gemäß Abschnitt 11 erfüllen. | Fotogelatine darf nur aus gemäß Abschnitt 11 zugelassenen Herkunftsbetrieben in den Vereinigten Staaten und in Japan eingeführt werden. | Anhang XV Kapitel 19 |
| 20 | Hörner und Hornprodukte (außer Hornmehl) sowie Hufe und Hufprodukte (außer Hufmehl) zur Herstellung von organischen Düngemitteln oder Bodenverbesserungsmitteln | Material der Kategorie 3 gemäß Artikel 10 Buchstaben a, b, h und n | Die Produkte müssen die Anforderungen gemäß Abschnitt 12 erfüllen. | Jedes Drittland | Anhang XV Kapitel 18 |
Abschnitt 213
Einfuhr von Blut und Blutprodukten, außer von Equiden, zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere
Für die Einfuhr von Blut und Blutprodukten, außer von Equiden, zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere gelten folgende Anforderungen:
1. Die Blutprodukte müssen aus einer Anlage zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere stammen, die den in der vorliegenden Verordnung festgelegten speziellen Bedingungen entspricht, oder aus dem Gewinnungsbetrieb.
2. Das Blut, aus dem Blutprodukte zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere hergestellt werden, muss unter tierärztlicher Aufsicht gewonnen worden sein:
3.1. Im Fall von Blutprodukten zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere, die von Tieren der Taxa Artiodactyla, Perissodactyla und Proboscidea oder von deren Kreuzungen gewonnen wurden, müssen entweder die in Buchstabe a oder die in Buchstabe b genannten Bedingungen erfüllt sein:
3.2. Zusätzlich zu Nummer 3.1 Buchstabe b Ziffern i und ii muss im Fall anderer Tiere als Suidae und Tayassuidae eine der folgenden Bedingungen erfüllt sein:
3.3. Zusätzlich zu Nummer 3.1 Buchstabe b Ziffern i und ii gilt im Fall von Suidae und Tayassuidae Folgendes: Im Herkunftsdrittland bzw. Herkunftsgebiet wurde seit mindestens zwölf Monaten kein Fall von vesikulärer Schweinekrankheit, klassischer Schweinepest oder afrikanischer Schweinepest gemeldet, seit mindestens zwölf Monaten wurde gegen keine dieser Krankheiten geimpft und eine der folgenden Bedingungen ist erfüllt:
4. Im Fall von Blutprodukten zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere, die von Geflügel oder anderen Vogelarten gewonnen wurden, müssen entweder die in Buchstabe a oder die in Buchstabe b genannten Bedingungen erfüllt sein:
Abschnitt 313
Einfuhr von Blut und Blutprodukten von Equiden Für die Einfuhr von Blut und Blutprodukten von Equiden gelten folgende Anforderungen:
1. Das Blut muss die Bedingungen gemäß Anhang XIII Kapitel IV Nummer 1 Buchstabe a erfüllen und unter tierärztliche Aufsicht entnommen werden, und zwar entweder:
2. Die Blutprodukte müssen die Bedingungen gemäß Anhang XIII Kapitel IV Nummer 2 erfüllen.
Ferner müssen die Blutprodukte gemäß Anhang XIII Kapitel IV Nummer 2 Buchstabe b Ziffer i aus Blut hergestellt worden sein, das Equiden entnommen wurde, die zumindest in den letzten drei Monaten vor dem Datum der Blutentnahme bzw. - falls die Tiere weniger als drei Monate alt sind - von Geburt an in tierärztlich beaufsichtigten Betrieben im Drittland der Blutentnahme gehalten wurden, das in diesem Zeitraum und während der Blutentnahme frei war von
3. Die Blutprodukte müssen aus einem Betrieb oder einer Anlage stammen, die von der zuständigen Behörde des Drittlandes zugelassen oder registriert wurde.
4. Das Blut und die Blutprodukte sind gemäß Anhang XIII Kapitel IV Nummer 3 zu verpacken und zu kennzeichnen.
Abschnitt 4
Einfuhr von Häuten und Fellen von Huftieren
Für die Einfuhr von Häuten und Fellen von Huftieren gelten folgende Anforderungen:
1. Frische oder gekühlte Häute und Felle dürfen eingeführt werden, wenn folgende Bedingungen erfüllt sind:
2. Behandelte Häute und Felle gemäß Anhang XIII Kapitel V Abschnitt C Nummer 2 dürfen ohne Einschränkung eingeführt werden.
3. Andere behandelte Häute und Felle dürfen eingeführt werden, wenn folgende Bedingungen erfüllt sind:
4. Frische, gekühlte oder behandelte Häute und Felle von Huftieren sind in Containern, Straßenfahrzeugen, Eisenbahnwaggons oder als Ballen einzuführen, die unter der Verantwortung der zuständigen Behörde des Versanddrittlandes verplombt wurden.
Abschnitt 5
Einfuhr von Jagdtrophäen und anderen Tierpräparaten
Für die Einfuhr von Jagdtrophäen und anderen Tierpräparaten gelten folgende Anforderungen:
1. Jagdtrophäen oder andere Tierpräparate, die die Bedingungen gemäß Anhang XIII Kapitel VI Abschnitt B und Abschnitt C Nummer 1 erfüllen, dürfen ohne Einschränkung eingeführt werden.
2. Behandelte Jagdtrophäen oder andere Präparate aus Vögeln und Huftieren, die ausschließlich aus Knochen, Hörnern, Hufen, Klauen, Geweihen, Zähnen, Häuten oder Fellen bestehen, aus Drittländern dürfen eingeführt werden, wenn sie die Anforderungen von Anhang XIII Kapitel VI Abschnitt C Nummer 1 Buchstabe a sowie Abschnitt C Nummer 2 Buchstabe a Ziffern i bis iii und Buchstabe b Ziffern i und ii erfüllen.
Jedoch brauchen trocken- oder nassgesalzene Häute und Felle, die auf dem Seeweg befördert werden, nicht 14 Tage vor ihrem Versand gesalzen zu werden, sofern sie 14 Tage vor ihrer Einfuhr gesalzen wurden.
3. Völlig unbehandelte Jagdtrophäen oder andere Präparate aus Vögeln und Huftieren, die aus ganzen Tierkörperteilen bestehen, dürfen unter folgenden Bedingungen eingeführt werden:
Abschnitt 6
Einfuhr von behandelten Federn, Federteilen und Daunen
Behandelte Federn, Federteile und Daunen dürfen unter folgenden Bedingungen eingeführt werden:
Abschnitt 7
Einfuhr von Knochen und Knochenprodukten (außer Knochenmehl), Hörnern und Hornprodukten (außer Hornmehl) sowie Hufen und Hufprodukten (außer Hufmehl), die zu anderen Zwecken als zur Verwendung als Futtermittel-Ausgangserzeugnisse, organische Düngemittel oder Bodenverbesserungsmittel bestimmt sind15 20
1. Knochen und Knochenprodukte (außer Knochenmehl), Hörner und Hornprodukte (außer Hornmehl) sowie Hufe und Hufprodukte (außer Hufmehl), dürfen zur Herstellung von Folgeprodukten zur Verwendung außerhalb der Futtermittelkette unter folgenden Bedingungen eingeführt werden:
2. Jeder Sendung muss ein Handelspapier beiliegen, das von der für die Überwachung des Herkunftsbetriebs zuständigen Behörde abgestempelt ist und folgende Angaben enthält:
3. Das Material muss in verplombten Containern oder Fahrzeugen oder als Massengut in einem Schiffsladeraum in die Union versandt werden.
Bei der Beförderung in Containern müssen diese sowie in jedem Fall alle Begleitpapiere Namen und Anschrift des registrierten Bestimmungsbetriebs bzw. der registrierten Bestimmungsanlage tragen.
4. Nach der in der Richtlinie 97/78/EG vorgesehenen Veterinärkontrolle und gemäß den Bestimmungen von Artikel 8 Absatz 4 der genannten Richtlinie ist das Material auf direktem Wege zum registrierten Bestimmungsbetrieb bzw. zur registrierten Bestimmungsanlage zu befördern.
Abschnitt 8
Einfuhr tierischer Nebenprodukte zur Herstellung von Pelztierfutter, Heimtierfutter außer rohem Heimtierfutter und Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere
Tierische Nebenprodukte, die zur Herstellung von Pelztierfutter, Heimtierfutter außer rohem Heimtierfutter und Folgeprodukten zur Verwendung außerhalb der Futtermittelkette für Nutztiere bestimmt sind, dürfen unter folgenden Bedingungen eingeführt werden:
1. Die tierischen Nebenprodukte wurden im Herkunftsbetrieb tiefgefroren oder gemäß den Unionsvorschriften so konserviert, dass sie zwischen dem Versand und der Anlieferung im Bestimmungsbetrieb bzw. in der Bestimmungsanlage nicht verderben können.
2. Es wurden alle Vorsichtsmaßnahmen getroffen, um eine Kontamination der tierischen Nebenprodukte mit Krankheitserregern zu vermeiden.
3. Die tierischen Nebenprodukte wurden in neuen, lecksicheren Verpackungen oder in Verpackungen, die vor der Verwendung gereinigt und desinfiziert worden sind, verpackt.
4. Nach der in der Richtlinie 97/78/EG vorgesehenen Veterinärkontrolle und gemäß Artikel 8 Absatz 4 der genannten Richtlinie erfolgt die Beförderung der tierischen Nebenprodukte auf direktem Wege entweder zu
5.1. im Fall von Rohmaterial zur Produktion von Heimtierfutter gemäß Artikel 35 Buchstabe a Ziffer ii der Verordnung (EG) Nr. 1069/2009 müssen folgende Bedingungen erfüllt sein:
5.2. besteht eine Sendung aus Rohmaterial, das gemäß Nummer 5.1 behandelt wurde, sowie aus anderem, nicht behandeltem Rohmaterial, wurden alle Rohmaterialien der Sendung gemäß Nummer 5.1 Buchstaben a und b gekennzeichnet;
5.3. die in Nummer 5.1 Buchstaben a und b sowie Nummer 5.2 vorgesehene Kennzeichnung muss während der gesamten Zeit vom Versand bis zur Anlieferung im Bestimmungsproduktionsbetrieb für Heimtierfutter sichtbar sein.
6. Im Bestimmungsproduktionsbetrieb für Heimtierfutter müssen die Lagerung vor Produktion, die Verwendung und die Beseitigung von Rohmaterial für die Heimtierfutterproduktion gemäß Artikel 35 Buchstabe a Ziffer ii der Verordnung (EG) Nr. 1069/2009 unter den von der zuständigen Behörde genehmigten Bedingungen erfolgen, die gegebenenfalls amtliche Kontrollen des Umfangs des gelieferten, des zur Produktion verwendeten und des beseitigten Materials umfassen.
Die zuständige Behörde kann dem Betreiber des Heimtierfutterbetriebs die Genehmigung erteilen, solche Materialien zusammen mit Material der Kategorie 3 zu lagern.
Abschnitt 9
Einfuhr ausgeschmolzener Fette für bestimmte Zwecke außerhalb der Futtermittelkette für Nutztiere13 20
Ausgeschmolzene Fette, die nicht zur Herstellung von Futtermitteln für Nutztiere, Kosmetika, Arzneimitteln oder Medizinprodukten bestimmt sind, dürfen unter folgenden Bedingungen eingeführt werden:
Abschnitt 10
Einfuhr von Fettderivaten
1. Fettderivate dürfen eingeführt werden, wenn die Veterinärbescheinigung, die der Sendung beiliegt, folgende Angaben enthält:
2. Die Veterinärbescheinigung gemäß Nummer 1 ist der zuständigen Behörde an der Grenzkontrollstelle des Eingangs der Erzeugnisse in die Union vorzulegen, anschließend muss eine Kopie die Sendung bis zu ihrer Ankunft im Bestimmungsbetrieb begleiten.
3. Nach der in der Richtlinie 97/78/EG vorgesehenen Veterinärkontrolle und gemäß den Bestimmungen von Artikel 8 Absatz 4 der genannten Richtlinie sind die Fettderivate auf direktem Wege zum registrierten Bestimmungsbetrieb bzw. zur registrierten Bestimmungsanlage zu befördern.
Abschnitt 11
Einfuhr von Fotogelatine
1. Gelatine, die aus Material hergestellt wurde, das Rinderwirbelsäule aus Material der Kategorie 1 gemäß Artikel 8 Buchstabe b der Verordnung (EG) Nr. 1069/2009 enthält, und die für die Fotoindustrie bestimmt ist ("Fotogelatine"), darf eingeführt werden, wenn die Fotogelatine
Tabelle 3 Einfuhr von Fotogelatine
| Herkunftsdrittland | Herkunftsbetriebe | Bestimmungsmitgliedstaat | Grenzkontrollstelle des Eingangs in die Union | Zugelassene Fotobetriebe |
| Japan | Nitta Gelatin Inc., 2-22 Futamata Yao-City, Osaka, 581-0024 Japan
Jellie Co. Ltd-7-1, Wakabayashi 2-Chome, Wakabayashiku, Sendai-City, NIPPI Inc. Gelatine Division |
Niederlande | Rotterdam | Fujifilm Europe, Oudenstaart 1, 5047 TK Tilburg, Niederlande |
| Nitta Gelatin Inc., 2-22 Futamata Yao-City, Osaka, 581-0024 Japan | Vereinigtes Königreich | Liverpool Felixstowe Heathrow | Kodak Ltd. headstone Drive, Harrow, middlesex, HA4 4TY, Vereinigtes Königreich |
|
| Tschechische Republik | Hamburg | FOMa Bohemia spol. SRO Jana Krusinky 1604 501 04 Hradec Kralove, Tschechische Republik |
||
| Vereinigte Staaten | Eastman Gelatine Corporation, 227 Washington Street, Peabody, MA, 01960 USA Gelita North America, |
Vereinigtes Königreich | Liverpool Felixstowe Heathrow | Kodak Ltd. headstone Drive, Harrow, middlesex, HA4 4TY, Vereinigtes Königreich |
| Tschechische Republik | Hamburg | FOMa Bohemia spol. SRO Jana Krusinky 1604 501 04 Hradec Králove, Tschechische Republik |
2. Nach ihrer Einfuhr in den Bestimmungsmitgliedstaat darf die Fotogelatine nicht zwischen den Mitgliedstaaten gehandelt, sondern nur in dem zugelassenen Fotobetrieb desselben Bestimmungsmitgliedstaats und ausschließlich zu Zwecken der Fotoherstellung verwendet werden.
3. Nach der in der Richtlinie 97/78/EG vorgesehenen Veterinärkontrolle und gemäß den Bestimmungen von Artikel 8 Absatz 4 der genannten Richtlinie ist die Fotogelatine auf direktem Wege zum registrierten Bestimmungsfotobetrieb zu befördern.
4. Die Beförderung gemäß Nummer 3 muss in Fahrzeugen oder Containern erfolgen, in denen die Fotogelatine physisch von Erzeugnissen getrennt ist, die zur Verwendung als Lebens- oder Futtermittel bestimmt sind.
5. Der Betreiber des zugelassenen Bestimmungsfotobetriebs stellt sicher, dass jegliche Überschüsse oder Reste sowie sonstige Abfälle der Fotogelatine
6. Fotogelatine ist gemäß folgenden Anforderungen herzustellen:
Der pH-Wert ist dann anzupassen und das Material durch Filterung und Sterilisierung bei 138-140 °C vier Sekunden lang zu reinigen.
Wird ein Leck festgestellt, sind Fahrzeug und Container gründlich zu reinigen und vor der Wiederverwendung zu inspizieren.
Abschnitt 12
Einfuhr von Hörnern und Hornprodukten (außer Hornmehl) sowie Hufen und Hufprodukten (außer Hufmehl), die zur Herstellung von organischen Düngemitteln oder Bodenverbesserungsmitteln bestimmt sind
Hörner und Hornprodukte (außer Hornmehl) sowie Hufe und Hufprodukte (außer Hufmehl), die zur Herstellung von Bodenverbesserungsmitteln oder organischen Düngemitteln bestimmt sind, dürfen unter folgenden Bedingungen eingeführt werden:
Kapitel III
Sondervorschriften für bestimmte Proben
Abschnitt 1
Proben für Forschungs- und Diagnosezwecke
Sofern Proben für Forschungs- und Diagnosezwecke sowie Produkte, die aus der Verwendung solcher Proben resultieren, nicht zu Referenzzwecken aufbewahrt oder in das Herkunftsdrittland zurückgesandt werden, sind sie wie folgt zu beseitigen:
Abschnitt 2
Handelsmuster
1. Die zuständige Behörde kann die Einfuhr und Durchfuhr von Handelsmustern unter folgenden Bedingungen genehmigen:
2. Sofern die Handelsmuster nicht zu Referenzzwecken aufbewahrt werden, sind sie
3. Werden Handelsmuster zur Prüfung von Maschinen verwendet, erfolgt die Prüfung
Bei der Beförderung zum zugelassenen oder registrierten Betrieb bzw. zur zugelassenen oder registrierten Anlage müssen die Handelsmuster in lecksicheren Containern verpackt sein.
Abschnitt 3
Ausstellungsstücke
1. Die Einfuhr und Durchfuhr von Ausstellungsstücken unterliegt folgenden Bedingungen:
2. Jede Sendung muss in lecksicheren Verpackungen verpackt sein, und ihr muss ein Handelspapier mit folgenden Angaben beiliegen:
3. Nach Ausstellungsende bzw. nach Abschluss der künstlerischen Tätigkeit sind Ausstellungsstücke
Kapitel IV
Spezielle Anforderungen an bestimmte Verbringungen tierischer Nebenprodukte
Abschnitt 1
Einfuhr bestimmten Materials der Kategorie 1
Material gemäß Artikel 26 darf unter folgenden Bedingungen eingeführt werden:
1. Das Material trägt bei der Einfuhr auf der Verpackung, dem Container oder dem Fahrzeug die Aufschrift "Nicht zur Verwendung in Lebensmitteln, Futtermitteln, Düngemitteln, Kosmetika, Arzneimitteln und Medizinprodukten".
2. Das Material wird auf direktem Wege an einen zugelassenen oder registrierten Betrieb bzw. eine zugelassene oder registrierte Anlage zur Herstellung von Folgeprodukten, ausgenommen Produkte gemäß Nummer 1, geliefert.
3. Nicht verwendetes oder überschüssiges Material wird gemäß Artikel 12 der Verordnung (EG) Nr. 1069/2009 verwendet oder beseitigt.
Abschnitt 2
Einfuhr bestimmten Materials zu anderen Zwecken als zur Verfütterung an Nutz-Landtiere
1. Die zuständige Behörde kann die Einfuhr folgenden Materials zu anderen Zwecken als zur Verfütterung an Nutz- Landtiere, ausgenommen zur Verfütterung an Pelztiere, genehmigen, sofern kein unannehmbares Risiko der Übertragung von Krankheiten auf Mensch oder Tier besteht:
2. Für die Einfuhr von Sendungen mit Material gemäß Nummer 1 müssen Veterinärbescheinigungen gemäß den nationalen Bestimmungen vorgelegt werden.
Kapitel V
Vorschriften für die Ausfuhr bestimmter Folgeprodukte17 20
Vorschriften für die Ausfuhr der nachstehend aufgeführten Folgeprodukte gemäß Artikel 25 Absatz 4:
| Folgeprodukte | Vorschriften für die Ausfuhr | |
| 1 |
|
Die folgenden Folgeprodukte müssen mindestens die Bedingungen gemäß Anhang XI Kapitel I Abschnitt 2 Buchstaben a, b, d und e erfüllen:
|
| 2 | Blutprodukte und Zwischenprodukte | Blut, Blutprodukte und Zwischenprodukte, die in der EU hergestellt oder gemäß den in Anhang XII oder Kapitel II Abschnitte 2 und 3 dieses Anhangs festgelegten Gesundheitsanforderungen zurVerwendung außerhalb der Futtermittelkette für Nutztiere bestimmt sind, sofern sie den Einfuhranforderungen des Bestimmungsdrittlandes entsprechen. |
Kapitel VI
Anforderungen an den Eingang von Sendungen von tierischen Nebenprodukten und Folgeprodukten, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen der Eingang in ein Drittland verwehrt wurde20
Abschnitt 1
Unverpackte oder lose tierische Nebenprodukte und Folgeprodukte, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen von einem Drittland bzw. Teil eines Drittlands, das bzw. der nicht in Anhang XIV aufgeführt ist, der Eingang verweigert wurde20
1. Die zuständige Behörde an der Grenzkontrollstelle genehmigt nur dann den Eingang in die Union von unverpackten oder losen tierischen Nebenprodukten und Folgeprodukten, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen von einem Drittland bzw. Teil eines Drittlands, das bzw. der nicht in Anhang XIV aufgeführt ist, der Eingang verweigert wurde, wenn folgende Bedingungen erfüllt sind:
2. Wurde abweichend von Nummer 1 Buchstabe a die Sendung ohne begleitende amtliche Bescheinigung oder begleitendes amtliches Dokument ausgeführt, erfolgt die Authentifizierung der Sendung in anderer Weise auf der Grundlage von Unterlagen, die von dem für die Sendung verantwortlichen Unternehmen bereitgestellt wurden.
3. Die Beförderung von Sendungen von unter Nummer 1 genannten Produkten von der Grenzkontrollstelle bis zum Bestimmungsort wird gemäß Artikel 2 der Delegierten Verordnung (EU) 2019/1666 überwacht.
Abschnitt 2
Unverpackte oder lose tierische Nebenprodukte und Folgeprodukte, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen von einem in Anhang XIV Drittland bzw. Teil eines Drittlands, das bzw. der in Anhang XIV aufgeführt ist, der Eingang verweigert wurde20
1. Die zuständige Behörde an der Grenzkontrollstelle genehmigt nur dann den Eingang in die Union von unverpackten oder losen tierischen Nebenprodukten und Folgeprodukten, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen von einem Drittland bzw. Teil eines Drittlands, das bzw. der in Anhang XIV aufgeführt ist, der Eingang verweigert wurde, wenn die unter Abschnitt 1 Nummer 1 Buchstaben a, b und c Ziffer ii sowie unter den Nummern 2 und 3 genannten Bedingungen erfüllt sind.
2. Wurden die unter Nummer 1 genannten Produkte entladen, gelagert oder umgeladen, oder wurde das Originalsiegel beim Eingang in das Drittland oder in einen Teil seines Hoheitsgebiets, das bzw. der in Anhang XIV aufgeführt ist, ersetzt, so wird der Sendung eine amtliche Erklärung der zuständigen Behörde oder einer anderen Behörde des betreffenden Drittlandes oder Gebiets beigefügt:
Abschnitt 3
Verpackte tierische Nebenprodukte und Folgeprodukte, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen der Eingang in ein Drittland verwehrt wurde20
1. Die zuständige Behörde an der Grenzkontrollstelle genehmigt nur dann den Eingang in die Union von verpackten tierischen Nebenprodukten und Folgeprodukten, die ihren Ursprung in der Union haben und in die Union zurückkehren, nachdem ihnen von einem Drittland der Eingang verweigert wurde, wenn die in Abschnitt 1 genannten Bedingungen erfüllt sind und die individuelle Verpackung der Produkte im Vergleich zu ihrem Zustand vor der Ausfuhr unversehrt geblieben ist.
2. Wurden die unter Nummer 1 genannten Produkte in einem Drittland entladen, muss der Sendung eine amtliche Erklärung der zuständigen Behörde oder einer anderen Behörde beiliegen, in der Folgendes bestätigt wird:
1) Durchführungsverordnung (EU) 2019/1715 der Kommission vom 30. September 2019 mit Vorschriften zur Funktionsweise des Informationsmanagementsystems für amtliche Kontrollen und seiner Systemkomponenten ("IMSOC -Verordnung") (ABl. L 261 vom 14.10.2019 S. 37).
| Muster-Veterinärbescheinigungen | Anhang XV17 19 |
Die Muster-Veterinärbescheinigungen in diesem Anhang gelten für die Einfuhr in und die Durchfuhr durch die Europäische Union der in den jeweiligen Muster-Veterinärbescheinigungen bezeichneten tierischen Nebenprodukte und Folgeprodukte aus Drittländern
Erläuterungen
| a) Das ausführende Drittland stellt die Veterinärbescheinigungen nach den im vorliegenden Anhang für die betreffenden tierischen Nebenprodukte vorgesehenen Mustern aus. Sie enthalten (in der im Muster vorgegebenen Reihenfolge) die für das betreffende Drittland erforderlichen Bescheinigungen und umfassen gegebenenfalls die für das Ausfuhrdrittland oder für einen Teil des Ausfuhrdrittlandes erforderlichen zusätzlichen Garantien.
b) Wenn aus der Muster-Veterinärbescheinigung hervorgeht, dass bestimmte Teile gegebenenfalls zu streichen sind, kann der/die Bescheinigungsbefugte nichtzutreffende Passagen durchstreichen, mit seinen/ihren Initialen versehen und stempeln, oder die entsprechenden Passagen werden vollständig aus der Veterinärbescheinigung entfernt. c) Das Bescheinigungsoriginal besteht aus einem einzelnen, beidseitig bedruckten Blatt oder, falls mehr Text erforderlich ist, aus mehreren Blättern, die alle ein zusammenhängendes, untrennbares Ganzes bilden müssen. d) Die Bescheinigung ist in mindestens einer der Amtssprachen des Mitgliedstaats, in dem die Grenzkontrolle stattfindet, und des Bestimmungsmitgliedstaates auszustellen. Diese Mitgliedstaaten können jedoch andere Gemeinschaftssprachen als ihre eigenen zulassen, wobei gegebenenfalls eine amtliche Übersetzung beiliegen muss. e) Werden der Bescheinigung zwecks Identifizierung der die Sendung ausmachenden Waren weitere Blätter beigefügt, so gelten auch diese als Teil des Bescheinigungsoriginals, und jedes einzelne dieser Blätter muss mit Unterschrift und Stempel des/der bescheinigungsbefugten amtlichen Tierarztes/Tierärztin versehen sein. |
f) Umfasst die Bescheinigung, einschließlich zusätzlicher Stückverzeichnisse gemäß Buchstabe e, mehrere Seiten, so ist jede Seite am Seitenende mit einer Nummerierung - (Seitenzahl) von (Gesamtseitenzahl) - und am Seitenkopf mit der von der zuständigen Behörde zugeteilten Codenummer zu versehen.
g) Das Bescheinigungsoriginal ist von einem amtlichen Tierarzt/einer amtlichen Tierärztin auszufüllen und zu unterzeichnen. Dabei tragen die zuständigen Behörden des Ausfuhrlandes dafür Sorge, dass die angewandten Bescheinigungsvorschriften den diesbezüglichen Vorschriften der Richtlinie 96/93/EG gleichwertig sind. h) Die Unterschrift muss sich farblich von der Druckfarbe der Bescheinigung abheben. Diese Vorschrift gilt auch für Amtssiegel, bei denen es sich nicht um Trockenstempel oder ein Wasserzeichen handelt. i) Das Bescheinigungsoriginal muss die Sendung bis zur Ankunft an der Grenzkontrollstelle der Union begleiten. j) Werden Veterinärbescheinigungen für die Durchfuhr von Sendungen verwendet, sind in Feld I.5. ("Empfänger") der Bescheinigung Name und Anschrift der Grenzkontrollstelle anzugeben, an der die Sendung die Europäische Union bestimmungsgemäß verlässt. |
Kapitel 117 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmtem verarbeitetem tierischem Protein, ausgenommen solches aus Nutzinsekten, einschließlich solches verarbeitetes tierisches Protein enthaltende Mischungen und Produkte, ausgenommen Heimtierfutter
 |
 |
 |
 |
 |
 |
Kapitel 1a17 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmtem verarbeitetem tierischem Protein aus Nutzinsekten, einschließlich solches Protein enthaltende Mischungen und Produkte, ausgenommen Heimtierfutter
 |
 |
 |
 |
 |
 |
Kapitel 2(A)19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von Milch, Erzeugnissen auf Milchbasis und aus Milch gewonnenen Erzeugnissen, die nicht zum menschlichen Verzehr bestimmt sind
 |
 |
 |
 |
 |
 |
Kapitel 2(B)19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von Kolostrum und Kolostrumerzeugnissen von Rindern, das/die nicht zum menschlichen Verzehr bestimmt ist/sind
 |
 |
 |
 |
Kapitel 3(A)19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von Heimtierfutter in Dosen
 |
 |
 |
 |
 |
Kapitel 3(B)13 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von verarbeitetem Heimtierfutter, ausgenommen Heimtierfutter in Dosen
 |
 |
 |
 |
 |
 |
 |
 |
Kapitel 3(C)19
Veterinärbescheinigung
für die Einfuhr in oder Durchfuhr durch 2 die Europäische Union von Kauspielzeug
 |
 |
 |
 |
 |
Kapitel 3(D)13 13a 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von rohem Heimtierfutter für den Direktverkauf oder von tierischen Nebenprodukten zur Verfütterung an Pelztiere
 |
 |
 |
 |
 |
 |
Kapitel 3(E)19
Veterinärbescheinigung
die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von geschmacksverstärkenden Fleischextrakten zur Verwendung bei der Herstellung von Heimtierfutter
 |
 |
 |
 |
 |
Kapitel 3(F)13 13a 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr 3 durch die Europäische Union von tierischen Nebenprodukten 2 für die Herstellung von Heimtierfutter
 |
 |
 |
 |
 |
 |
Kapitel 4(A)13
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von Blut und Blutprodukten von Equiden für Verwendungszwecke außerhalb der Futtermittelkette
 |
 |
 |
 |
Kapitel 4(B)15 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmten Blutprodukten, die als Einzelfuttermittel verwendet werden könnten
 |
 |
 |
 |
 |
 |
Kapitel 4(C)13 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von unbehandelten Blutprodukten, ausgenommen von Equiden, zur Herstellung von Folgeprodukten für Verwendungszwecke außerhalb der Futtermittelkette für Nutztiere
 |
 |
 |
 |
 |
 |
Kapitel 4(D)13 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von behandelten Blutprodukten, ausgenommen von Equiden, zur Herstellung von Folgeprodukten für Verwendungszwecke außerhalb der Futtermittelkette für Nutztiere
 |
 |
 |
 |
 |
Kapitel 5(A)
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von frischen oder gekühlten Häuten und Fellen von Huftieren



Kapitel 5(B)
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von behandelten Häuten und Fellen von Huftieren



Kapitel 5(C)
Amtliche Erklärung
für die Einfuhr in oder die Durchfuhr durch (1) die Europäische Union behandelter Häute und Felle von Wiederkäuern und Equiden, die vor der Einfuhr 21 Tage lang getrennt gehalten wurden oder mindestens 21 Tage ohne Unterbrechung befördert werden



Kapitel 6(A)13
Veterinärbescheinigung
für die Einfuhr in und die Durchfuhr durch (2) die Europäische Union von behandelten Jagdtrophäen und anderen Präparaten von Feder- und Schalenwild, die ausschließlich aus Knochen, Hörnern, Hufen, Klauen, Geweihen, Zähnen, Häuten oder Fellen bestehen
 |
 |
 |
|
Kapitel 6(B)19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von aus ganzen Tierkörperteilen bestehenden unbehandelten Jagdtrophäen und anderen Präparaten von Feder- und Schalenwild
 |
 |
 |
 |
 |
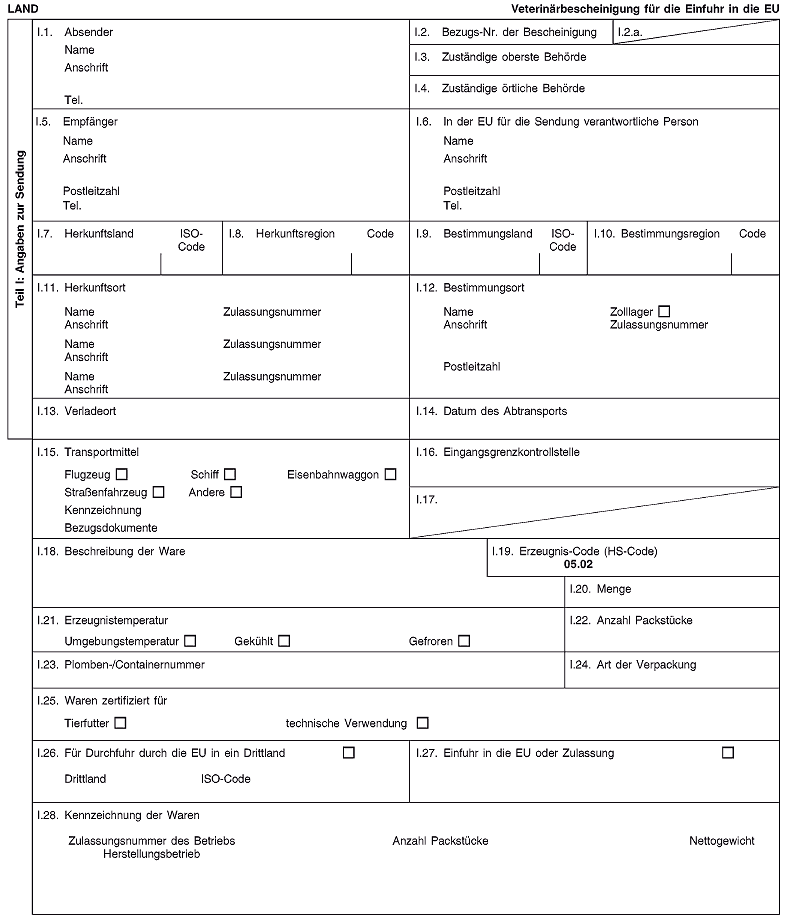
Kapitel 7(A)
Veterinärbescheinigung
für die Einfuhr in und die Durchfuhr durch (2) die Europäische Union von Schweinsborsten aus Drittländern oder Drittlandgebieten, in denen die afrikanische Schweinepest nicht vorkommt

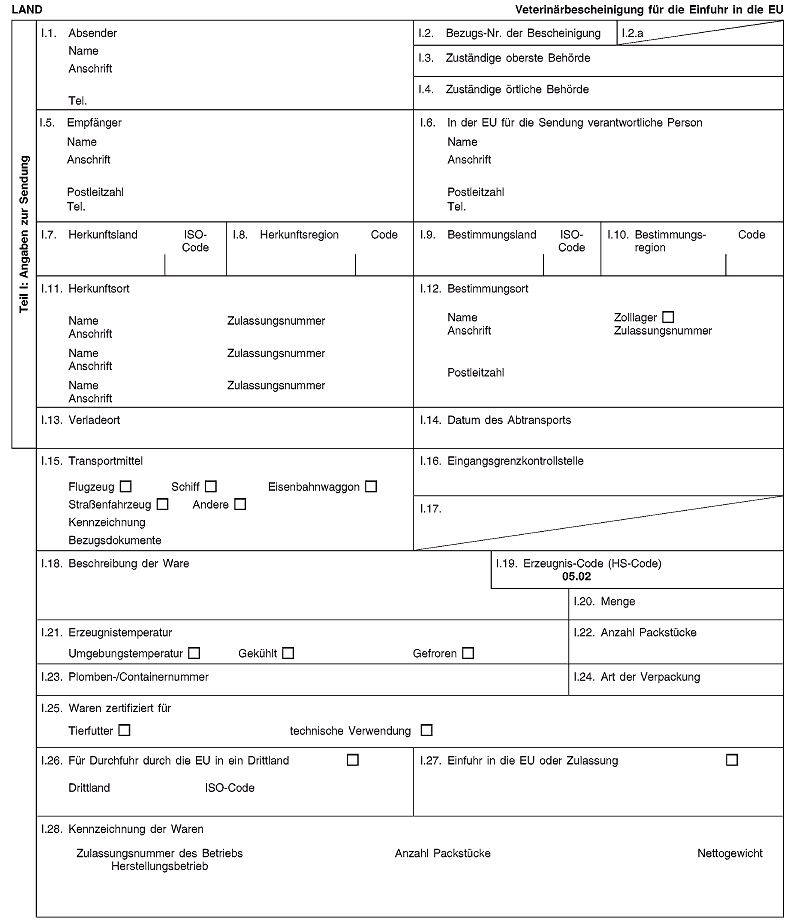
Kapitel 7(B)
Veterinärbescheinigung
für die Einfuhr in und die Durchfuhr durch (2) die Europäische Union von Schweinsborsten aus Drittländern oder Drittlandgebieten, in denen die afrikanische Schweinepest vorkommt


Kapitel 813 13a 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von tierischen Nebenprodukten zur Verwendung außerhalb der Futtermittelkette oder als Handelsmuster 2
 |
 |
 |
 |
 |
 |
 |
 |
Kapitel 9
Veterinärbescheinigung
für die Einfuhr in und die Durchfuhr durch (2) die Europäische Union von nicht zum menschlichen Verzehr bestimmtem Fischöl zur Verwendung als Futtermittel-Ausgangserzeugnis oder für Verwendungszwecke außerhalb der Futtermittelkette
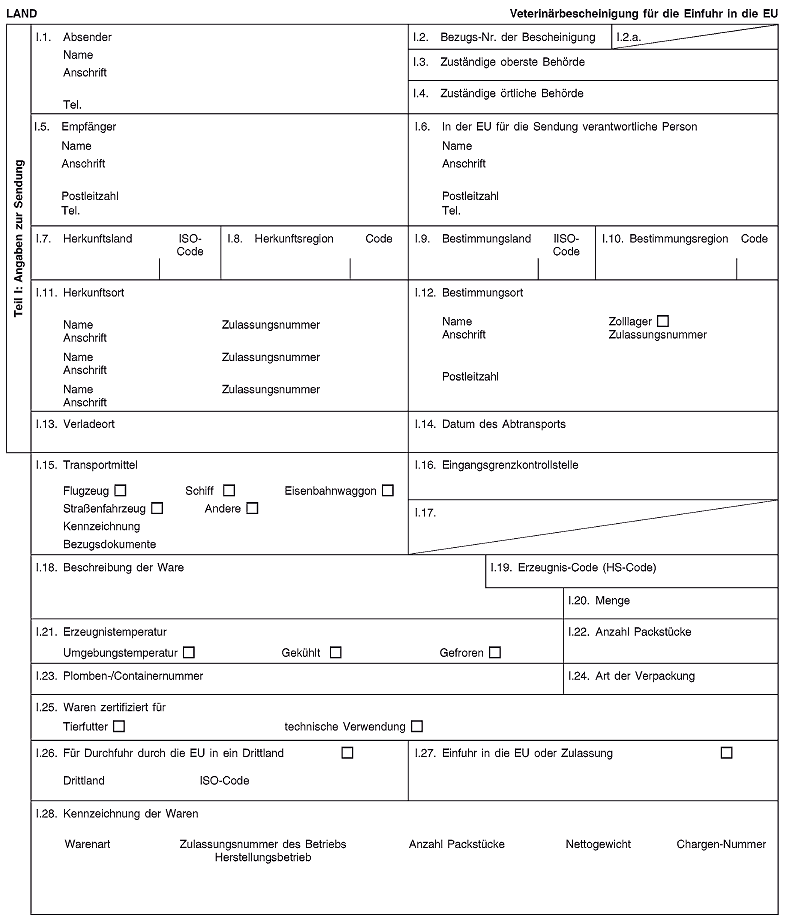


Kapitel 10(A)19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmten ausgeschmolzenen Fetten, zur Verwendung als Einzelfuttermittel
 |
 |
 |
 |
 |
 |
Kapitel 10(B) 13 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmten ausgeschmolzenen Fetten, für bestimmte Verwendungszwecke außerhalb der Futtermittelkette
 |
 |
 |
 |
 |
 |
Kapitel 1113 19
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmter Gelatine/bestimmtem Kollagen zur Verwendung als Einzelfuttermittel oder für Verwendungszwecke außerhalb der Futtermittelkette
 |
 |
 |
 |
 |
 |
Kapitel 1219
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von nicht zum menschlichen Verzehr bestimmtem hydrolisiertem Protein, Dicalciumphosphat und Tricalciumphosphat zur Verwendung als Einzelfuttermittel oder für Verwendungszwecke außerhalb der Futtermittelkette
 |
 |
 |
 |
 |
 |
Kapitel 13
Veterinärbescheinigung
für die Einfuhr in und die Durchfuhr durch (2) die Europäische Union von ausschließlich zur Verwendung in der Imkerei bestimmten Imkerei-Nebenprodukten
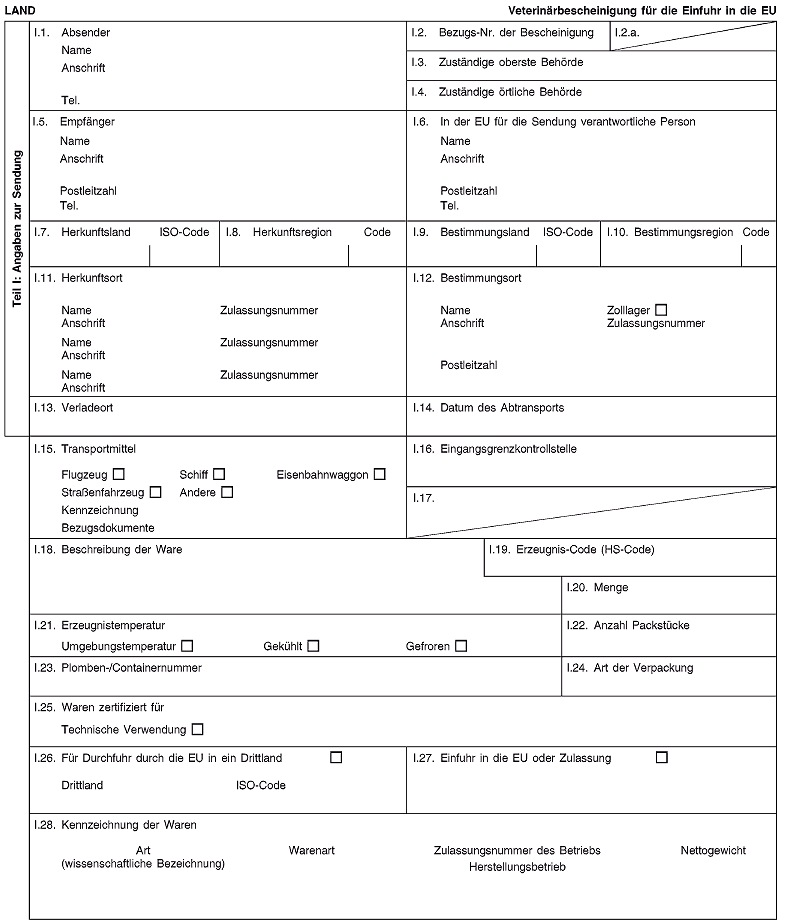

Kapitel 14(A)13
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von nicht zum menschlichen Verzehr bestimmten Fettderivaten, zur Verwendung außerhalb der Futtermittelkette
 |
 |
 |
 |
Kapitel 14(B)
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von nicht zum menschlichen Verzehr bestimmten Fettderivaten, zur Verwendung als Futtermittel oder außerhalb der Futtermittelkette



Kapitel 1513
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch (2) die Europäische Union von nicht zum menschlichen Verzehr bestimmten Eiprodukten, die als Futtermittel-Ausgangserzeugnisse verwendet werden können
 |
 |
 |
|
Kapitel 16
Mustererklärung
Erklärung des Eiführers/der Einführerin von Knochen und Knochenprodukten (ausgenommen Knochenmehrl), Hörnern und Hornprodukten (ausgenommen Hornmehl) sowie Hufen und Hufprodukten (ausgenommen Hufmehl), die nicht zur Verwendung als Futtermittel-Ausgangserzeugnisse, organische Düngemittel oder Bodenverbesserungesmittel bestimmt sind, in die Europäische Union.
Hinweis für den Einführer/ie Einführerin: Diese Erklärung dient ausschließlich Veterinärzwecken und muß die Sendung bis zur Grenzkontrollstelle begleiten.
Der/Die Unterzeichente erklärt, dass die nachstehend bezeichneten Produkte (1):
a) Knochen und Knochenprodukte(ausgenommen Knochenmehl),
b) Hörner und Hornprodukte (ausgenommen Hornmehl),
c) Hufe und Hufprodukte (ausgenommen Hufmehl)
dazu bestimmt sind, von ihm/ihr in die Union eingeführt zu werden, jedoch zu keinem Zeitpunkt in Lebensmitteln, Futtermitteln, organischen Düngemitteln oder Bodenverbesserungsmitteln verwendet werden, und dass sie auf direktem Wege zur weiteren Verarbeitung bzw. Behandlung gesendet werden an:
Name ................................................................. Adresse .....................................................................
Außerdem erkläre ich, dass das Produkt weder spezifiziertes Risikomaterial im Sinne des Anhangs V der Verordnung (EG) Nr. 999/2001 noch Separatorenfleisch von Knochen von Rindern, Schafen oder Zeigen enthält und auch nicht aus solchem Material oder solchem Fleisch gewonnen wurde.
Der Einführer
Name ................................................................. Adresse ..................................................................................
Geschehen zu .................................................... am ............................................................................................
(Ort) (Datum)
Unterschrift ..................................................
Bezugsnummer wie im Gemeinsamen Veterinärdokument für die Einfuhr (GVDE) gemäß Anhang III der Verordnung (EG) Nr. 136/2004 der Kommission angegeben:
................................................................................................................................................................................
Amtssiegel der Grenzkontrollstelle am Ort des Eingangs ins Hoheitsgebiet der Europäischen Union (2)
Unterschrift ..............................................................................................................................................................
(Unterschrift des amtlichen Tierarztes/der amtlichen Tierärztin der Grenzkontrollstelle) (2)
Name ......................................................................................................................................................................
(Name in Großbuchstaben)
Kapitel 17
Veterinärbescheinigung
für die Einfuhr in die oder die Durchfuhr durch (2) die Europäische Union von verarbeiteter Gülle, aus dieser gewonnenen Folgeprodukten und Guano von Fledermäusen



Kapitel 1819
Veterinärbescheinigung
für die Einfuhr in oder die Durchfuhr durch 2 die Europäische Union von Hörnern und Hornprodukten (außer Hornmehl) sowie Hufen und Hufprodukten (außer Hufmehl), die zur Herstellung organischer Düngemittel oder Bodenverbesserungsmittel bestimmt sind
 |
 |
 |
 |
Kapitel 19
Veterinärbescheinigung
für die Einfuhr in die Europäische Union von nicht zum menschlichen Verzehr bestimmter Gelatine zur Verwendung in der Fotoindustrie



Kapitel 2015 19
Mustererklärung
Erklärung für die Einfuhr aus Drittländern und die Durchfuhr durch 2 die Europäische Union von Zwischenprodukten, die zur Herstellung von Arzneimitteln, Tierarzneimitteln, Medizinprodukten für ärztliche und tierärztliche Zwecke, aktiven implantierbaren medizinischen Geräten, In-vitro-Diagnostika für ärztliche und tierärztliche Zwecke, Laborreagenzien und kosmetischen Mittel bestimmt sind
 |
 |
 |
 |
 |
Kapitel 21
Mustererklärung
Erklärung des Einführers unbehandelter Wolle und unbehandelter Haare gemäß Artikel 25 Absatz 2 Buchstabe e für die Einfuhr in die Europäische Union

| Amtliche Kontrollen | Anhang XVI14 |
Kapitel I
Amtliche Kontrollen in Verarbeitungsbetrieben
Abschnitt 1
Überwachung der Produktion
1. Die zuständige Behörde überwacht die Verarbeitungsbetriebe, um sicherzustellen, dass die Anforderungen der Verordnung (EG) Nr. 1069/2009 und der vorliegenden Verordnung eingehalten werden.
Sie
2. Die zuständige Behörde muss zu allen Bereichen des Verarbeitungsbetriebs sowie zu Büchern, Handelspapieren und Veterinärbescheinigungen jederzeit freien Zugang haben, um die ihr nach Nummer 1 obliegenden Aufgaben wahrnehmen zu können.
Abschnitt 2
Validierungsverfahren
1. Vor Erteilung einer Zulassung für einen Verarbeitungsbetrieb gemäß Artikel 44 Absatz 1 der Verordnung (EG) Nr. 1069/2009 hat die zuständige Behörde zu prüfen, ob der Unternehmer eine Validierung des Verarbeitungsbetriebs gemäß den folgenden Verfahren und Indikatoren durchgeführt hat:
2. Bei Chargenbetrieb unter Dampfdruckbedingungen ist
Thermoelement und Druckmesser sind mindestens einmal jährlich zu eichen.
3. Bei kontinuierlicher Arbeitsweise unter Dampfdruckbedingungen
Die genaue Bestimmung und Kontrolle der Durchlaufrate ist unerlässlich und erfolgt im Rahmen des Validierungstests an einer fortlaufend überwachbaren kritischen Stelle durch Messung:
Alle Mess- und Überwachungsgeräte müssen mindestens einmal jährlich geeicht werden.
4. Die zuständige Behörde muss die Kontrollen der Validierungsverfahren immer dann wiederholen, wenn sie dies für erforderlich hält, in jedem Fall jedoch immer dann, wenn der Verarbeitungsprozess wesentlich geändert wurde (z.B. andere Maschinen oder anderes Rohmaterial).
Kapitel II
Listen der registrierten und zugelassenen Anlagen, Betriebe und Unternehmer
1. Zugang zu den Listen der registrierten und zugelassenen Anlagen, Betriebe und Unternehmer
Um die Mitgliedstaaten bei der Bereitstellung aktueller, den anderen Mitgliedstaaten und der Öffentlichkeit zugänglicher Listen registrierter und zugelassener Anlagen, Betriebe und Unternehmer zu unterstützen, richtet die Kommission eine Website mit Links zu den nach Nummer 2 Buchstabe a erstellten nationalen Websites der einzelnen Mitgliedstaaten ein.
2. Format nationaler Websites
3. Die Gestaltung der Hauptlisten, einschließlich der einschlägigen Informationen und Codes, erfolgt nach den technischen Spezifikationen, die die Kommission auf ihrer Website veröffentlicht.
Kapitel III
Besondere Vorschriften für amtliche Kontrollen
Abschnitt 1
Amtliche Kontrollen der Kennzeichnung von Folgeprodukten
Die zuständige Behörde führt eine Leistungsprüfung des Überwachungs- und Aufzeichnungssystems gemäß Anhang VIII Kapitel V Nummer 2 der vorliegenden Verordnung durch, um deren Einhaltung zu überprüfen, und kann erforderlichenfalls die Untersuchung zusätzlicher Proben nach der in Absatz 2 der genannten Nummer festgelegten Methode fordern.
Abschnitt 2
Amtliche Kontrollen in Verbrennungsanlagen mit niedriger Kapazität
Die zuständige Behörde hat eine Abfallverbrennungsanlage mit niedriger Kapazität zur Verbrennung spezifizierten Risikomaterials vor deren Zulassung und mindestens einmal jährlich zu inspizieren, um die Einhaltung der Verordnung (EG) Nr. 1069/2009 und der vorliegenden Verordnung zu überwachen.
Abschnitt 3
Amtliche Kontrollen in abgelegenen Gebieten
Im Fall der Beseitigung tierischer Nebenprodukte in entlegenen Gebieten gemäß Artikel 19 Absatz 1 Buchstabe b der Verordnung (EG) Nr. 1069/2009 überwacht die zuständige Behörde in regelmäßigen Abständen die als entlegene Gebiete eingestuften Gebiete, um sicherzustellen, dass diese Gebiete und die Beseitigungsvorgänge ordnungsgemäß kontrolliert werden.
Abschnitt 4
Amtliche Kontrollen in registrierten Pelztierhaltungsbetrieben
1. Die zuständige Behörde ergreift die erforderlichen Maßnahmen zur Kontrolle
2. Die in Nummer 1 Buchstabe b Ziffer ii genannten Proben müssen Proben von Tieren umfassen, die neurologische Symptome aufweisen, sowie solche von älteren Zuchttieren.
Abschnitt 5
Amtliche Kontrollen von Sammelstellen
1. Die zuständige Behörde veranlasst Folgendes:
2. Die zuständige Behörde führt in Sammelstellen amtliche Kontrollen durch, um die Einhaltung der vorliegenden Verordnung zu überprüfen.
Abschnitt 613
Amtliche Kontrollen der Verfütterung von Material der Kategorie 1 an wildlebende Tiere und bestimmte Zootiere
Die zuständige Behörde überwacht den Gesundheitszustand der Nutztiere in der Region, in der gemäß Anhang VI Kapitel II Abschnitte 2, 3 und 4 gefüttert wird, und führt eine angemessene TSE-Überwachung einschließlich regelmäßiger Entnahme von Proben und deren Untersuchung auf TSE durch.
Diese Proben müssen Proben von verdächtigen Tieren umfassen sowie solche von älteren Zuchttieren.
Abschnitt 7
Amtliche Kontrollen der Ausbringung bestimmter organischer Düngemittel und Bodenverbesserungsmittel
Die zuständige Behörde führt Kontrollen entlang der gesamten Herstellungs- und Verwendungskette von organischen Düngemitteln und Bodenverbesserungsmitteln durch, die den Beschränkungen gemäß Anhang II Kapitel II unterliegen.
Bei diesen Kontrollen sind auch die Mischung mit einem in Anhang XI Kapitel II Abschnitt 1 Nummer 2 genannten Bestandteil sowie die Bestände solcher Produkte in landwirtschaftlichen Betrieben und die gemäß der Verordnung (EG) Nr. 1069/2009 und der vorliegenden Verordnung zu führenden Aufzeichnungen zu kontrollieren.
Abschnitt 8
Amtliche Kontrollen zugelassener Fotobetriebe
Die zuständige Behörde führt in den in Anhang XIV Kapitel II Abschnitt 11 Nummer 1 Tabelle 3 genannten zugelassenen Fotobetrieben Dokumentenkontrollen zur Kanalisierungskette von der Grenzkontrollstelle der ersten Einführung bis zu den zugelassenen Fotobetrieben durch, um die Mengen der eingeführten, verwendeten und entsorgten Produkte abzugleichen.
Abschnitt 9
Amtliche Kontrollen bestimmter eingeführter ausgeschmolzener Fette
Die zuständige Behörde führt in den registrierten Betrieben oder Anlagen, die nach Anhang XIV Kapitel II Abschnitt 9 eingeführte ausgeschmolzene Fette annehmen, Dokumentenkontrollen zur Kanalisierungskette von der Grenzkontrollstelle der ersten Einführung bis zum registrierten Betrieb oder der registrierten Anlage durch, um die Mengen der eingeführten, verwendeten und entsorgten Produkte abzugleichen.
Abschnitt 1012 19
Standardformat für Anträge auf bestimmte Genehmigungen im Handel innerhalb der Union
Die Unternehmer informieren unter Verwendung des folgenden Formats in TRACES die zuständige Behörde des Ursprungsmitgliedstaats und beantragen bei der zuständigen Behörde des Bestimmungsmitgliedstaats die Genehmigung des Versands von tierischen Nebenprodukten und von ihren Folgeprodukten gemäß Artikel 48 Absatz 1 der Verordnung (EG) Nr. 1069/2009 sowie von zur Entgiftung bestimmtem Fischöl oder Fischmehl aus Material der Kategorie 3:
 |
 |
Erläuterungen:
Bitte in GROSSBUCHSTABEN ausfüllen.
(1) Zutreffendes bitte ankreuzen.
(2) Im Fall von aus Material der Kategorie 1 hergestelltem Heimtierfutter, das aus tierischen Nebenprodukten von Tieren besteht, die einer vorschriftswidrigen Behandlung gemäß Artikel 1 Absatz 2 Buchstabe d der Richtlinie 96/22/EG oder Artikel 2 Buchstabe b der Richtlinie 96/23/EG unterzogen wurden;
(3) Angabe gemäß Artikel 18 der Verordnung (EG) Nr. 1069/2009.
(4) Gegebenenfalls ausfüllen.
(5) Bitte angeben.
(6) Bitte eine der in Anhang IV Kapitel III der Verordnung (EU) Nr. 142/2011 genannten Verarbeitungsmethoden angeben.
(7) Für die zuständige Behörde: Zutreffendes bitte ankreuzen.
(8) Datum des Ablaufs der Genehmigung einfügen.
Abschnitt 1115
Amtliche Kontrollen in Bezug auf Hydrolyse mit anschließender Beseitigung
Die zuständige Behörde führt an Standorten, an denen Hydrolyse mit anschließender Beseitigung durchgeführt wird, Kontrollen gemäß Anhang IX Kapitel V Abschnitt 2 Buchstabe B durch.
Bei solchen Kontrollen ist zum Zwecke des Abgleichs der versandten und der beseitigten Mengen hydrolisierten Materials eine Dokumentenprüfung vorzunehmen
Während der ersten zwölf Betriebsmonate ist am Standort des Behälters für die Hydrolyse ein Kontrollbesuch jedes Mal dann durchzuführen, wenn dem Behälter hydrolisiertes Material entnommen wird.
Nach diesen ersten zwölf Betriebsmonaten findet ein solcher Kontrollbesuch jedes Mal dann statt, wenn der Behälter geleert und auf Korrosion und Leckage gemäß Anhang IX Kapitel V Abschnitt 2 Buchstabe B Nummer 3 Buchstabe j untersucht wird.
Abschnitt 1214 17
Amtliche Kontrollen in Bezug auf für die Verbrennung von tierischen Nebenprodukten zugelassene Anlagen
Die zuständige Behörde nimmt in zugelassenen Anlagen gemäß Anhang III Kapitel V im Einklang mit den in Artikel 6 Absatz 7 und Artikel 8 genannten Verfahren Dokumentenprüfungen vor.
 |
ENDE |  |
(Stand: 19.11.2020)
Alle vollständigen Texte in der aktuellen Fassung im Jahresabonnement
Nutzungsgebühr: 90.- € netto (Grundlizenz)
(derzeit ca. 7200 Titel s.Übersicht - keine Unterteilung in Fachbereiche)
Die Zugangskennung wird kurzfristig übermittelt
? Fragen ?
Abonnentenzugang/Volltextversion